Hidrocefalia
Definición
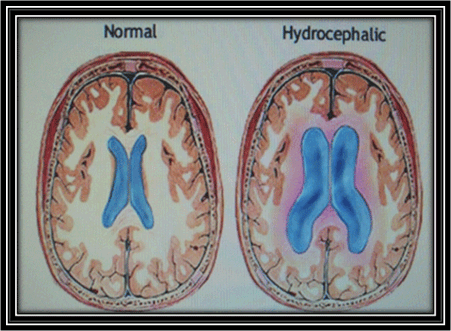
La hidrocefalia es un trastorno de la dinámica del líquido cefalorraquídeo (LCR), que provoca la anormal expansión de los ventrículos cerebrales.
Como indica su nombre, es una condición en la que la principal característica es la acumulación excesiva de líquido en el cerebro, que provoca una dilatación anormal de los ventrículos y / o el espacio subaracnoideo 1).
Historia
 El término hidrocefalia deriva de las palabras griegas “hidro” que significa agua y “céfalo” que significa cabeza.
El término hidrocefalia deriva de las palabras griegas “hidro” que significa agua y “céfalo” que significa cabeza.
Aunque la hidrocefalia se conocía antiguamente como “agua en el cerebro”, el “agua” es en realidad líquido cefalorraquídeo.
Walter Dandy, en colaboración con KD Blackfan, del Departamento de Pediatría, llevó a cabo estudios experimentales en perros, que lo condujeron a concluir que la obstrucción: del agujero de Monro, el acueducto de Silvio, o de las cisternas alrededor del tronco cerebral, causarían el hidrocéfalo y la disminucion de la absorcion del LCR.
El estudio de la fisiopatología comenzó con el trabajo de Walter Dandy y Blackfan en las primeras décadas del siglo XX 2).
La radiografía simple y la punción lumbar fueron los únicos estudios, que se podían realizar.
Más tarde Dandy desarrolló la ventriculografía.
El primer trabajo apareció en 1913, en el JAMA cuando Dandy tenía 27 años, a los 32 introdujo la ventriculografía en 1918 y un año después la neumoencefalografía, lo que le dio un gran impulso a la neurocirugía por la precisión que aportaba en la localización de los procesos intracraneanos.
La confrontación que luego se dio, determinó que Cushing fuera poco receptivo en adoptar la ventriculografía en el Peter Bent Brigham Hospital. Según las cartas de Dandy a sus padres, las investigaciones en el laboratorio “eran suyas”. En ellas menciona que Cushing iba poco al laboratorio, y cuando lo hacía era para señalar que los experimentos que él había planeado eran probablemente proclives a no llevarse a cabo.
Epidemiología
Es más común en los bebés, que en los adultos.
La prevalencia estimada de hidrocefalia se sitúa en torno al 1-1,5%, siendo la incidencia de la hidrocefalia congénita de 0,9 a 1,8/1000 nacimientos.
Clasificación
No existe consenso internacional sobre la clasificación de la hidrocefalia, existiendo diversos sistemas, basadas en la edad de comienzo, dinámica del LCR y zona anatómica del acúmulo, los niveles de presión del LCR, y la presencia de síntomas.
En este sentido, la hidrocefalia puede ser:
Hidrocefalia obstructiva (no comunicante)
Según los ventrículos afectados
Tipos según etiología
Las causas más frecuentes de hidrocefalia son las hemorragias intracerebrales (hemorragia subaracnoidea, hemorragia intraventricular), las malformaciones (Chiari, estenosis de acueducto de Silvio), las infecciones (meningitis, ventriculitis) y los tumores.
Hidrocefalia idiopática y no idiopática
Etiología de la hidrocefalia no idiopática:
1. Hidrocefalia posthemorrágica
3. Postmeningítica dentro de la hidrocefalia adquirida
4. Secundaria a una intervención de la fosa posterior
5. Tumores, incluida la meningitis carcinomatosa
6. también observada en 15% de los pacientes que padecen DSSA (enfermedad de Alzheimer)
7. defecto de absorción de las granulaciones aracnoidales
8. la estenosis del acueducto puede ser una causa no valorada adecuadamente.
1) Lesiones Congénitas:
A) Obstruction o estenosis de A. de Silvio
a) Gliosis
b) Forkin
c) Estenosis verdadera
d) Septum
B) Atresia del foramen de Luschka y Magendie
(Dandy Walker)
C) Masas:
a) Quistes intracraneano Benignos
b) M.A.V.
c) Tumores
2) Lesiones Adquiridas
A) Estenosis de acueductos de Silvio (Gliosis)
B) Inflamaciones ventriculares y cicatrices
C) Masas:
a) Tumores
b) Masa no neoplastica
D) Craneo
a) Platibasia
b)Acondroplasia
Hidrocefalia Comunicante
1.-Lesiones Congénitas
a) Malformaciones de Chiari
b) Encefalocele
c) Inflamacion de Leptomeninges
d) Lisencefalia
e) Ausencia congénita de vellocidades aracnoideas
2.- Lesiones Adquiridas
A) Inflamaciones de Leptomeninges:
a) Infecciones
b) Hemorragias
c) Cuerpos extranos
B) Masas
a) Tumores
b) No neoplasticas
3.- Hipersecresión de LCR.
a) Papilomas de plexo coroideo
4.- Misceláea
a) Deficiencia vitamínica: complejo B
b) Toxinas en período embrionario
c) Drogas: Esteroides, vitamina A, AC. Valpróico y otros.
d) Genéticas
5. Idiopáticas
Las hidrocefalias se deben a un defecto de la reabsorción del LCR o, con menor frecuencia, a una superproducción de LCR (como ocurre en presencia de algunos papilomas de los plexos coroideos; incluso en estos casos, la reabsorción probablemente también sea defectuosa en cierto grado, puesto que es probable que los individuos sanos toleren el ligero aumento de producción del LCR que provocan estos tumores).
Congénita Las causas congénitas no malformativas son múltiples, entre ellas enumeramos las fetopatias, la toxoplasmosis congénita y la infección por citomegalovirus. Las hidrocefalias secundarias a lesiones destructivas isquémicas son raras.
Las hidrocefalias congénitas se revelan principalmente en el período neonatal y rara vez en la adolescencia; pueden ser de origen malformativo en su gran mayoría, infecciosa, vascular o criptogenética. A. malformación de Chiari II o mielomeningocele (habitualmente, son concurrentes)
B. malformación de Chiari I: la hidrocefalia puede presentarse junto con obstrucción de los orificios de salida del cuarto ventrículo
La malformación de Arnold Chiari aumenta la resistencia a la circulación del LCR a nivel de la fosa posterior. La agenesia del foramen de Monro es rara, al igual que la agenesia de los puntos de absorción del LCR (Síndrome de Meckel y síndrome de Vactrel). Las hidrocefalias genéticas o familiares se asocian a anomalías cromosómicas del 8,9,13,18,21. C. estenosis primaria del acueducto (por lo general, se observa en niños, raramente en adultos.)Las malformaciones que producen estenosis no tumoral del acueducto de Sylvius conforman el 10% de las hidrocefalias del recién nacido y su incidencia es del 0.5 al 1 por 1000. Se describen 4 tipos: Agenesia total o parcial del acueducto. Acueducto reemplazado por varios canalículos. Acueducto tapado por un septum ependimario. La estenosis del acueducto es rara, y puede asociarse a otras malformaciones. D. gliosis secundaria del acueducto: a causa de una infección intrauterina o de una hemorragia de la matriz germinal. E. malformación de Dandy-Walker (atresia de los agujeros de Luschka y Magendie): la incidencia de esta malformación entre los pacientes que padecen hidrocefalia es de 2,4%. La malformación de Dandy Walker produce obstrucción a la salida del IV ventrículo. F. poco frecuente: trastornos congénitos ligados al cromosoma X.
Adquirida A. infecciosa (es la causa más frecuente de hidrocefalia comunicante)
Las meningitis originan el 7% de las hidrocefalias del lactante. Todas las meningitis bacterianas pueden producirla, (sobre todo, la purulenta y la basal, incluida la tuberculosa que la puede cursar de forma crónica.)por adherencias aracnoideas y estenosis del acueducto de Silvio.
Un obstáculo anatómico o funcional a nivel de los senos venosos, puede originar raramente hidrocefalia, cuando la bóveda craneana es aun compliante; las causas son múltiples. Son igualmente raras la hidrocefalia iatrogénica, la producida por hipervitaminosis
A. Un sangrado o meningitis desapercibida o parcialmente tratada, pueden explicar los casos sin etiología evidente.
2. cisticercosis
B. poshemorrágica (segunda causa más frecuente de hidrocefalia comunicante)
1. por HSA.
2. por hemorragia intraventricular: en muchos pacientes, se presenta una hidrocefalia transitoria. Entre 20% y 50% de los pacientes que padecieron una gran hemorragia intraventricular presentan después hidrocefalia permanente.
C. secundaria a lesiones ocupantes
Los procesos expansivos (tumor, quiste, hematoma…) son la causa del 20% de las hidrocefalias de los niños, excepcionalmente se trata de un tumor del plexo coroide; la localización mas frecuente es la fosa posterior, la región pineal y mesencefálica por su cercanía al acueducto de Silvius y las lesiones del tercer ventrículo.
Tumor de la pineal en un niño con hidrocefalia grave
Los quistes supraselares, el aneurisma de la vena de Galeno y rara vez un tumor de la medula espinal son causas también de hidrocefalia.
El 15% de las hidrocefalias tienen como causa una hemorragia intracraneal (trauma, malformación, prematuridad). En la fase aguda puede haber un coagulo en la vía de drenaje, pero mas frecuentemente se produce obstrucción por depósitos de fibrina sobre los espacios subaracnoideos y los sitios de absorción. 1. no neoplásicas: p. ej., malformaciones vasculares
2. neoplásicas: la mayoría provoca hidrocefalia obstructiva porque bloquea las vías del LCR.
D. posquirúrgica: 20% de los pacientes pediátricos presenta hidrocefalia permanente (que requiere una derivación) después de extirparles un tumor de la fosa posterior. Puede tardar hasta un año en presentarse E. neurosarcoidosis F. “ventriculomegalia estructural”: es asintomática y no requiere ningún tratamiento. G. asociada a tumores medulares.
Etiología en el adulto
Las causas son muy variadas y numerosas, pueden ser congénitas o adquiridas:
La hemorragia meníngea (HSAE): Es la causa mas frecuente, generalmente por la ruptura de un aneurisma intracraneano. Un tercio de las HSAE se complican con hidrocefalia aguda, y 10% producen hidrocefalia sintomática de forma crónica. Se explica la hidrocefalia, por aumento de la viscosidad del LCR por la sangre de la hemorragia, por adherencias en los sitios de absorción y por obstrucción en los casos de taponamiento agudo.
Meningitis: Menos frecuentes que las anteriores, las etiologías son: Bacteriana, tuberculosa, linfomatosa y carcinomatosa. El mecanismo es semejante a la HSAE. Una ependimitis, en el caso de las bacterianas, puede originar una estenosis del acueducto o de los forámenes intraventriculares.
Trauma de cráneo e intervenciones quirúrgicas: En particular en los ancianos, el mecanismo, conjuga las dos etiologías anteriores.
Tumores: Se explica por obstrucción de las vías de drenaje del LCR a nivel ventricular, y por aumento de la viscosidad del LCR en los casos de tumores de la medula espinal. Las etiologías son múltiples predominando los tumores intraventriculares, paraselares y de la región de la pineal y la fosa posterior.
Tumor maligno de la lámina cuadrigeminal, Mostrando una gran dilatación de los ventrículos laterales
Estenosis no tumoral del acueducto: Difícil de explicar en el adulto, pude ser congénito pero parece haber siempre una causa secundaria no bien diagnosticada. Se desconoce el límite a partir del cual la estenosis se convierte en sintomática.
Otras causas: Las malformaciones de Dandy Walker, Chiari, quistes aracnoideos de la base, la sífilis, el síndrome de Guillain Barré y la enfermedad de Paget, son causas menos frecuentes de hidrocefalia.
Etiopatogenia
Los trastornos en la producción, circulación y absorción del LCR son las causas que provocan una dilatación del sistema ventricular, principalmente las dos últimas.
La hiperproducción de LCR se ha observado únicamente en el papiloma del plexo coroideo.
Fisiopatología
La fisiopatología de la hidrocefalia se encuentra en la dinámica de la circulación del líquido cefalorraquídeo. El consiguiente estancamiento de LCR en la hidrocefalia interfiere con el desarrollo cerebral 3).
En teoría, la hidrocefalia puede aparecer por tres mecanismos: una hiperproducción de LCR, un aumento de la resistencia de la circulación de LCR, o un aumento de la resistencia a la absorción por aumento de la presión venosa.
Existe una teoría en la que se podría producirse una falta de absorción debido a la inmadurez cerebral en recién nacidos y lactantes (1).
La consecuencia de cualquiera de los tres mecanismos es un aumento en la presión del LCR para mantener el equilibrio entre la secreción y la absorción. Por lo tanto, la dilatación ventricular no es el resultado de la desigualdad entre secreción y absorción sino, que ella es secundaria al aumento de presión hidrostática de LCR. Los mecanismos que preceden la dilatación del sistema son multifactoriales e intervienen en diferentes momentos de su formación. Es probable que el mecanismo inicial sea la compresión del sector vascular y una modificación de la distribución del LCR y los líquidos extracelulares. A largo plazo, es la destrucción tisular la que contribuye a la dilatación de los ventrículos. De otro lado en el niño y el joven existe un aumento del volumen del cráneo por la fuerza anormal sobre las suturas craneales.
Hiperproducción de LCR
Es debida casi exclusivamente a los tumores del plexo coroide (papiloma o carcinoma). La hiperproducción de LCR por sí sola produce una hipertensión intracraneal e hidrocefalia, pero también pueden contribuir la compresión en las vías de drenaje y la formación de adherencias por microhemorragias. Rara vez la hipervitaminosis A puede explicar una hiperproducción de LCR.
Obstáculo a la circulación del LCR
Es la causa de la mayoría de las hidrocefalias. El aumento en la resistencia creada por el obstáculo lleva a un aumento proporcional en la presión del LCR para mantener la absorción.
Estas hidrocefalias se clasifican según la localización del obstáculo: no comunicantes, cuando el obstáculo es ventricular y comunicantes cuando el obstáculo esta mas allá de los ventrículos, como en los problemas de taponamiento en los sitios de absorción que determinan una hidrocefalia tanto interna como externa.
Fases de la hidrocefalia
Inicio
En condiciones normales existe un equilibrio entre las presiones del LCR, el parénquima cerebral y el espacio subaracnoideo. Cuando aparece el obstáculo que aumenta la resistencia a la circulación, y el LCR continua su producción y su débito, se aumenta la presión dentro de los ventrículos y se establece un gradiente de presión hacia el parénquima y el espacio subaracnoideo
Fase aguda
El gradiente de presión establecido, origina una fuerza radial que dilata los ventrículos. El parénquima cerebral, comparado con un material visco-elástico (con la edad se torna más plástico que elástico) sufre esfuerzos tangenciales que determinan un daño mecánico.
El espacio subaracnoideo se colapsa y se vacía, poniendo la corteza en contacto con la duramadre y la bóveda ósea, infinitamente menos compliante que el parénquima, (a excepción del recién nacido y del lactante, por sus suturas aun abiertas) recibiendo la casi totalidad de la fuerza radial expansiva. La dilatación para, equilibrando las presiones a niveles cada vez mas altos, hasta que sobre viene la muerte del paciente.
Fase crónica
La mayoría de las hidrocefalias no evolucionan hacia la hipertensión intracraneana terminal, tienden a volverse crónicas, coexistiendo una presión aparentemente normal y la dilatación. Esta evolución puede explicarse por diferentes mecanismos:
Parece haber una disminución en la producción de LCR; de otro lado, existe un aumento progresivo de las capacidades de absorción:
La distensión ventricular origina disyunción de las células ependimarias, explicando la reabsorción transependimaria.
Igualmente a través de los espacios perivasculares y de los nervios craneanos.
Estos mecanismos hacen que el gradiente y la hidrocefalia paren, la presión se torna normal, con una dilatación ventricular fija de grado variable y sobretodo, asintomática.
En algunos casos la situación se agrava, con presiones normales o ligeramente altas, pero con ondas patológicas de hipertensión (ondas A o B) El gradiente de presión transependimaria mantiene o agrava la dilatación, al mismo tiempo que en el parénquima cerebral se alteran las propiedades mecánicas por cambios en su composición y estructura.
Clínica
Las formas de presentación varían de acuerdo a la edad y las circunstancias del diagnóstico.
En el lactante y recién nacido
La macrocefalia es el signo mas evidente y frecuente, está presente en todas las hidrocefalias crónicas en los menores de 2 años y se define como un crecimiento del cráneo mayor de 2 desviaciones Standard, lo cual sirve en el diagnóstico diferencial con la macrocefalia constitucional donde el crecimiento craneal permanece en la misma faja de desviación.
A las hidrocefalias se asocian signos de hipertensión intracraneana: Abombamiento de la fontanela anterior, separación de las suturas craneanas, la piel del cráneo es fina y brillante. La parálisis de los músculos rectos superiores con el signo del sol poniente o signo de Parinaud o un estravismo interno son la traducción de un daño del tectum del tallo cerebral. El edema papilar no es tan frecuente como lo son la atrofia y la disminución de la agudeza visual.
En el niño
El síndrome de hipertensión intracraneana aguda es mas frecuente en el niño y el adulto por la rigidez del cráneo. Se instala rápidamente y se traduce por cefalea, vómito, alteración de la conciencia y de los nervios oculomotores.
En los casos graves aparecen signos de sufrimiento del tallo cerebral, como crisis tónicas por herniación de las amigdalas cerebelosas, bradicardia, alteración del ritmo respiratorio, convirtiéndose en una urgencia neuroquírurgica.
Los casos crónicos
En el lactante, la macrocefalia se asocia a retraso mental en grado variable.
En el niño, después de cerradas las suturas, aparecen cefaleas progresivas en frecuencia, a veces se acompañan de dolor abdominal matinal, nauseas y vómito en proyectil. Aparecen además alteraciones del comportamiento, disminución en el rendimiento escolar y a veces alteraciones en la memoria.
En estados tardíos, aparecen alteraciones de la conciencia, como obnubilación y estupor. En esta fase los riesgos son la destrucción masiva del tejido cerebral y la atrofia óptica por destrucción del nervio.
Rara vez, se detectan en un niño macrocefalico: Espasticidad por daño del eje piramidal; esta origina alteraciones de la marcha y movimientos anormales. Las alteraciones endocrinas por compresión del eje hipotálamo-hipofisario en el tercer ventrículo son poco frecuentes y se traducen por un retardo del crecimiento, obesidad variable y alteraciones en los genitales externos.
Manifestaciones clínicas en el adulto
Síndrome de hipertensión intracraneana
Se presenta en los casos de hidrocefalia aguda o subaguda. La cefalea de aparición reciente y de localización difusa se hace progresiva y frecuente. El vómito es muy frecuente en los jóvenes con tumores de la fosa posterior.
El vértigo se puede acompañar de acúfenos. Alteraciones visuales como la diplopía, se explican por lesión del VI par; finalmente el edema papilar se traduce en visión borrosa y ceguera.
Otros síntomas mas inquietantes anuncian una deterioro fatal por herniación cerebral. Son mas frecuentes en los jóvenes con hidrocefalia aguda o descompensación de una hidrocefalia crónica. Alteraciones del tono muscular cervical explican una ligera inclinación lateral de la cabeza. Pueden aparecer crisis paroxísticas de hipertonía en opistótonos. La alteración de la conciencia evoluciona rápidamente hasta el coma y aparecen alteraciones vegetativas respiratorias, cardíacas y de la regulación térmica.
Ocasionalmente la hipertensión intracraneana evoluciona de forma crónica con signos que pueden pasar desapercibidos:
Alteraciones psiquiátricas (apatía, irritabilidad, déficit de atención y memoria, hipomanía).
Crisis epilépticas (generalizadas y en relación con alteraciones circulatorias).
Alteraciones endocrinas (hipopituitarismo).
Síndrome piramidal bilateral.
Disminución de la agudeza visual.
Diagnóstico
Criterios en TC y RM de la hidrocefalia.
Abreviaturas: DI = diámetro interno, AF = astas frontales, AT = astas temporales.
Es indicativa de hidrocefalia la presencia de algunos de los siguientes signos:
A. El tamaño de las astas temporales (AT) es > 2 mm de ancho (véase la Figura) (en ausencia de H, las astas temporales apenas son visibles) y la cisura de Silvio, la cisura interhemisférica y los surcos cerebrales no son identificables.
O bien
B. ambas AT son > 2 mm y la proporción
AF> 0,5 (en la que AF representa el ancho mayor de las astas frontales y DI Direpresenta el diámetro de tabla interna a tabla interna en ese nivel) (véase la Figura)
Otras características indicativas de hidrocefalia hidrostática:
1. “balonamiento” de las astas frontales y de los ventrículos laterales (figura del “Ratón Mickey”) y del tercer ventrículo.
2. hipodensidad periventricular en la TC o señal periventricular hiperintensa en el T2 de la RM, lo cual es indicativo de absorción transependimaria o migración de LCR.
3.Cociente AF/DI < 40% normal 40%-50% valor límite
50% indica hidrocefalia
4.Índice de Evans: proporción entre las AF y el diámetro biparietal máximo, (de tabla externa a tabla externa) > 30%.
5. La RM sagital puede mostrar un aumento de la curvatura superior del cuerpo calloso.
Perímetro cefálico Es fundamental controlar el perímetro cefálico de todo niño que está en etapa de crecimiento (como parte de la puericultura general y, en especial, en los niños en los que se sospecha la presencia de hidrocefalia y en quienes la hidrocefalia está comprobada). Como regla general, el perímetro cefálico de un lactante normal debe ser igual a la distancia existente entre el vértice de la cabeza y las nalgas.
Crecimiento normal de la cabeza: está expresado en las curvas normales.
Todos los hallazgos que se enumeran a continuación pueden indicar afecciones tratables —hidrocefalia activa, hematoma subdural o efusiones subdurales— y, por ende, deben llevar al médico a solicitar que se estudie al paciente con algún método que evalúe el contenido intracraneal (p. ej., TC, ecografía cerebral, etc.) 1. desviación hacia arriba (curvas que se cruzan) 2. crecimiento continuo de la cabeza de más de 1,25 cm por semana 3. perímetro cefálico que se acerca a 2 desviaciones estándar (D. E.) sobre las medidas normales 4. perímetro cefálico desproporcionado respecto de la altura o el peso del cuerpo, incluso si está dentro de los límites normales para la edad. Estas manifestaciones también se observan en los niños prematuros durante la fase compensadora del crecimiento cerebral que se produce después de que se recuperan de enfermedades agudas. En el niño prematuro y durante el período neonatal, pueden ser indicativas de microcefalia las desviaciones de menos de 0,5 cm por semana por debajo de las curvas de crecimiento de la cabeza (excepto durante las primeras semanas de vida). Técnica: se debe medir el perímetro rodeando la frente y el occipucio (sin las orejas) tres veces consecutivas y utilizar el valor más alto. Luego, se traslada este valor a un gráfico de valores medios normales en función de la edad. Cada paciente debe tener un gráfico propio en el cual se marque el crecimiento del perímetro cefálico.
Diagnóstico diferencial
Los estados que pueden ser similares a la hidrocefalia, pero que no se deben a una absorción inadecuada del LCR son: 1. atrofia: en algunas ocasiones denominada “hidrocefalia ex vacuo”, no representa ninguna alteración hidrodinámica del LCR, sino que constituye una pérdida de tejido cerebral. 2. hidranencefalia. 3. anomalías congénitas en las que los ventrículos están agrandados: A. agenesia del cuerpo calloso: (ocasionalmente, puede estar asociada a la hidrocefalia, pero más a menudo sólo se trata de una expansión del tercer ventrículo y una separación de los ventrículos laterales) B. displasia septoóptica: Signos y síntomas de la hidrocefalia activa En niños pequeños 1. el cráneo crece más rápidamente que el rostro 2. irritabilidad, mal control de la cabeza, náuseas y vómitos 3. fontanela tensa y protuberante 4. hipertrofia y congestión de las venas del cuero cabelludo: a causa del flujo retrógrado que, como consecuencia de un aumento de la PIC, proviene de los senos cerebrales. 5. signo de Macewen: ruido de olla cascada al percutir el cráneo (efecto sobre los ventrículos dilatados). 6. parálisis de VI par craneal (motor ocular externo): se ha postulado que su largo curso intracraneal lo hace muy sensible a los aumentos de presión intracraneana 7. “signo del sol poniente” (parálisis de la mirada hacia arriba): síndrome de Parinaud causado por la presión ejercida sobre la región del receso suprapineal 8. reflejos hiperactivos 9. respiración irregular con períodos de apnea 10. diástasis de las suturas del cráneo (visibles en radiografía simple) En niños mayores o en adultos que presentan rigidez de la bóveda craneal Se observan síntomas de aumento de la PIC: papiledema, cefalea, náuseas y vómitos, cambios en la marcha, parálisis de la mirada hacia arriba o del motor ocular externo. La dilatación lenta de los ventrículos puede ser asintomática en la etapa inicial.
A continuación, se describen las características que son indicativas de hidrocefalia crónica (en contraposición con la hidrocefalia aguda): 1. aumento de las impresiones digitiformes (también denominado “aspecto de cobre o plata martillada”, que puede observarse en las radiografías simples de cráneo22. Por sí solo, este signo no se correlaciona con una PIC aumentada, pero cuando está asociado a los puntos 3 y 4 de esta lista, es indicativo de T PIC. Se observa en casos de craneosinostosis. 2. hernia del tercer ventrículo que se adentra en la silla turca (se observa en TC o RM) 3. erosión de la silla turca (la causa puede ser el punto 2), que a veces provoca el síndrome de la silla turca vacía, y erosión de la lámina cuadrilátera del esfenoides 4. en la TC, las astas temporales pueden ser menos prominentes que en la hidrocefalia aguda 5. macrocefalia: por convención, perímetro cefálico mayor que 98VO percentil. 6. atrofia del cuerpo calloso: se aprecia mejor en la RM sagital 7. en los niños: A. diástasis de las suturas B. retraso en el cierre de las fontanelas C. retraso en el desarrollo o imposibilidad de crecimiento.
Hidrocefalia detenida
No hay acuerdo respecto de la definición exacta de este término y algunos lo utilizan como sinónimo de hidrocefalia compensada. La mayoria aplica de forma indistinta cualquiera de estos terminos para referirse a una situación en la que no hay avance de la dilatación ni aparicion de secuelas deletéreas claramente causadas por la hidrocefalia que requerirían la colocación de una derivacion del LCR. Es importante aconsejar a los padres y familiares que consulten con el medico de inmediato si los niños presentan síntomas de hipertension intracraneal (descompensación): cefalea, vomitos, ataxia o alteraciones de la vision. La hidrocefalia detenida satisface los siguientes criterios, en ausencia de una derivacion del LCR: 1. el tamaño de los ventrfculos es casi normal 2. la curva de crecimiento de la cabeza es normal 3. el desarrollo psicomotor es contínuo y no presenta anomalias.
Cuarto ventriculo atrapado (o aislado)
Como bien lo expresa su denominación, se trata de un cuarto ventriculo que no se comunica con el tercero (a traves del acueducto de Silvio) ni con las cisternas basales (a traves de los agujeros de Luschka y Magendie). Se observa, generalmente, en los pacientes que tienen una derivacion de los ventriculos laterales de larga evolución, en especial, en hidrocefalia secundaria a una infección (sobre todo, fúngica) o en quienes padecieron infecciones recurrentes de la derivación. Posiblemente, esta afección se genere como consecuencia de la formación de adherencias debido a la yuxtaposición prolongada de la íntima ependimaria del acueducto provocada por la ausencia de LCR que ha sido desviado a traves de la derivación. Los plexos coroideos del cuarto ventriculo continuan produciendo LCR, liquido que distiende el cuarto ventriculo cuando hay una obstrucción de los orificios de salida del cuarto ventriculo o un bloqueo a nivel de las granulaciones aracnoideas. Los sintomas iniciales pueden ser: 1. cefalea 2. parálisis de los pares craneales bajos: dificultades de la deglucion 3. ataxia 4. reducción del nivel de conciencia 5. náuseas o vómitos 6. tambien puede ser un hallazgo casual (algunos hallazgos “atípicos”, como la reducción del campo de atención, pueden estar relacionados) Tratamiento La mayoria de los cirujanos esta a favor de derivar el ventriculo, ya sea mediante otra derivacion ventriculoperitoneal (VP) o uniéndola a una derivacion existente. Una de las complicaciones posibles consiste en que, como consecuencia del drenaje del cuarto ventriculo, el tronco encefalico retorne a su position normal y pueda sufrir un daño tardio provocado por la punta del cateter. Es posible evitar esta complicación introduciendo el cateter a traves del hemisferio cerebeloso hacia el cuarto ventriculo, en forma paralela a su piso para que no se produzca angulacion del catete. Como alternativa, puede considerarse la colocación de una derivación lumboperitoneal (LP) si los orificios de salida del cuarto ventrículo están permeables. Si no lo están, puede realizarse una ventriculocisternostomía (derivación de Torkildsen).
Tratamiento
Frecuentemente se trata solo el síntoma y solo ocasionalmente la causa; cuando sea posible se debe tratar la causa, por ejemplo un tumor que obstruye la circulación del LCR o la repermeabilización de una estructura normalmente abierta.
Al tratamiento, generalmente quirúrgico, se asocia un tratamiento médico temporal para disminuir la evolución de la hidrocefalia. Este tratamiento basado en la acetazolamida y la furosemida (ambos inhibidores de la anhidrasa carbónica por mecanismos diferentes) debe ser transitorio y es ineficaz a largo plazo. Este tratamiento puede probarse en los niños prematuros en quienes el LCR es sanguinolento (siempre que no haya signos de hidrocefalia activa) mientras se observa si se reanuda la absorción normal del LCR. No obstante, en las mejores circunstancias, este tratamiento debe ser considerado un complemento del tratamiento definitivo o una medida contemporizadora. Según un estudio comparativo del año 1995, fue posible normalizar satisfactoriamente la hidrocefalia en « 50% de los pacientes menores de un año que tenían signos vitales estables, función renal normal y no presentaban síntomas de PIC aumentada (apnea, letargo, vómitos) utilizando los siguientes fármacos:
acetazolamida (inhibidor de la anhidrasa carbónica): 25 mg/kg/ día v.o. fraccionados en 3 dosis diarias x 1 día, aumentando 25 mg/kg/día cada día hasta llegar a los 100 mg/kg/día simultáneamente, iniciar un tratamiento con furosemida: 1 mg/kg/ día fraccionado en 3 dosis diarias para contrarrestar la acidosis: ♦ tricitrato (Polycitra®) (EE.UU.): 4 ml/kg/ día fraccionados en 4 dosis diarias (cada mi equivale a 2 mEq de bicarbonato y contiene 1 mEq de K+ y 1 mEq de Na+) ♦ realizar una medición seriada de los electrólitos y ajustar la dosis para mantener el nivel de HCO3 en suero > 18 mEq/1 ♦ reemplazar el fármaco con Polycitra-K® (EE. UU.) (2 mEq K+ por mi, no tiene Na+) si baja el nivel de potasio en suero, o con bicarbonato de sodio si baja el nivel de sodio en suero controlar que no se produzcan desequilibrios electrolíticos ni que se presenten EC de la acetazolamida: letargo, taquipnea, diarrea.
• realizar ecografías o TC semanales y efectuar una derivación ventricular si se presenta una ventriculomegalia progresiva. Si el paciente se mantiene estable, continuar con el tratamiento durante 6 meses de ensayo, luego reducir la dosis gradualmente a lo largo de 2-4 semanas. Reiniciar el tratamiento y mantenerlo durante 3-4 meses si se presenta hidrocefalia progresiva
Punción lumbar La hidrocefalia que se presenta después de una hemorragia intraventricular puede ser transitoria. Es posible contemporizar mediante punciones seriadas (ventriculares o lumbares) hasta que se reanude la resorción, pero sólo debe realizarse una PL en los casos de hidrocefalia comunicante. Si la reabsorción no se reanuda cuando la proteinorraquia es < 100 mg/dl, entonces es poco probable que se produzca una resolución espontánea (es decir, por lo general, es necesario colocar un sistema de derivación).
Tratamiento quirúrgico
Hasta la llegada de las técnicas endoscópicas el tratamiento casi exclusivamente empleado ha sido la derivación de LCR desde el sistema ventricular al atrio inicialmente, y al peritoneo con posterioridad.
El objetivo del tratamiento no consiste en lograr que los ventrículos vuelvan al tamaño normal, sino que la función neurológica sea óptima y el resultado estético sea satisfactorio. Las opciones de tratamiento son: 1. plexectomía coroidea: fue descripta por Dandy en el año 1918 como tratamiento de la hidrocefalia comunicante. Si bien mediante esta técnica es posible reducir el índice de producción del LCR, no la detiene por completo (los plexos coroideos segregan sólo una porción de la producción total de LCR, otras fuentes son el revestimiento ependimario de los ventrículos y las vainas durales de las raíces de los nervios raquídeos). La operación a cielo abierto fue asociada a un alto índice de mortalidad (quizás, debido a que el LCR es reemplazado por aire). La coagulación endoscópica de los plexos coroideos fue descrita originalmente en 1910 y ha resurgido recientemente. 2. eliminar la obstrucción: p. ej., canalizar un acueducto de Silvio estenosado. Presenta mayor morbilidad y tiene un índice de éxito menor que la operación simple de derivación, excepto, quizás, en los casos de tumores 3. ventriculostomía del tercer ventrículo. 4. derivación: más adelante se describen varios sistemas de derivación.(derivación ventriculoperitoneal y ventriculoauricular, derivación ventriculopleural y lumboperitoneal).
Ventrículocisternostomía bajo control endoscópico
Es el tratamiento de primera elección en la estenosis del acueducto de Silvio y consiste en comunicar, bajo control visual endoscópico, el III ventrículo con los espacios subaracnoideos de la base a nivel de la cisterna interpeduncular.Se ha renovado el interés en la ventriculostomía del tercer ventrículo gracias al uso más divulgado de la cirugía endoscópica (ventriculoscópica). Indicaciones: este procedimiento puede ser de utilidad para corregir la hidrocefalia obstructiva. Asimismo, es una opción para el tratamiento de la infección de la derivación (como un medio de retirar todo el material extraño sin someter al paciente a una intervención mayor). La ventriculostomía del tercer ventrículo también ha sido propuesta como opción para los pacientes en los que se forma un hematoma subdural después colocar una derivación (se retira el sistema de derivación antes de practicar el procedimiento). También puede ser de utilidad para tratar el síndrome del ventrículo en hendidura. Contraindicaciones: la hidrocefalia comunicante es una contraindicación absoluta para efectuar una ventriculostomía del tercer ventrículo. Las contraindicaciones relativas serían todas las enfermedades o estados que estén asociados a un bajo índice de resultados favorables.
Complicaciones: 1. daño hipotalámico 2. parálisis transitoria de los pares III y VI 3. hemorragia incoercible 4. paro cardíaco 5. aneurisma traumático de la arteria basilar: posiblemente esté relacionado con las heridas térmicas provocadas por el uso del láser cuando se lo utilizó para llevar a cabo la ventriculostomía. índice de resultados satisfactorios: el índice general de resultados satisfactorios es = 56% (con un margen de 60% a 94% para la estenosis del acueducto no tumoral). El mayor índice de mantenimiento de la permeabilidad se observa en las estenosis del acueducto adquiridas que no fueron tratadas anteriormente. En los niños, el índice de resultados satisfactorios puede llegar a ser bajo porque es probable que el espacio subaracnoideo no esté normalmente desarrollado. Este índice se reduce (sólo = 20% de las ventriculostomías permanecen permeables) en los casos que presentan enfermedades preexistentes: 1. tumores 2. derivación previa 3. HSA previa 4. radioterapia previa aplicada a todo el cerebro (se desconoce el índice de resultados satisfactorios de la radiocirugía estereotáctica focalizada) 5. importantes adherencias que son visibles al perforar el piso del tercer ventrículo en el momento de efectuar la ventriculostomía.
Visión endoscópica del foramen de Monro y el plexo coroide en el ventrículo lateral
Su ventaja consiste en evitar el implante de una prótesis de derivación pero requiere que los sitios de absorción de LCR estén permeables.
Es de elección también en el tratamiento de los quistes aracnoideos supraselares y de la cisura tentorial, ya que se puede comunicar el quiste que produce la obstrucción, con el sistema ventricular directamente.
Se han descrito mejorías radiológicas de hasta un 55 % en niños con hidrocefalia postmeningitis (2), pero su indicación fundamental estriba en las obstructivas en los que se pueda realizar de forma segura comunicación con el sistema ventricular.
La derivación externa del LCR
Consiste en colocar un catéter ventricular (generalmente en el cuerno frontal derecho) conectado a un sistema externo, con control por columna hidrostática del débito de LCR a ser drenado.
Es una solución de espera usada en los casos de hidrocefalia temporal en la HSAE aguda y en el tratamiento de una sobreinfección de sistemas de derivación. Posteriormente algunos de estos pacientes necesitarán una derivación definitiva del LCR.
Puede servir también para la conexión de un sistema de monitoreo y vigilancia de la PIC, en pacientes donde para indicar la colocación de una derivación definitiva necesita argumentos mas sólidos que el simple cuadro clínico.
Las derivaciones internas
Permite establecer una comunicación entre los ventrículos y una cavidad interna, por medio de un catéter con o sin interposición de una válvula subcutánea, reguladora de presión. La selección de la cavidad (peritoneo, aurícula derecha, pleura, vejiga, vesícula biliar) depende de cada paciente.
Sistemas de derivación
1. Derivación ventriculoperitoneal (VP): es la derivación más utilizada actualmente.La derivación ventrículo-peritoneal (del ventrículo a la cavidad peritoneal) es la preferida tanto en adultos como en niños debido a la facilidad para elongar el catéter según su crecimiento; además las complicaciones sépticas son más fáciles de tratar.
2.Derivación ventrículoatrial:(del ventrículo al atrio cardíaco derecho) es el sitio de segunda elección en el niño, ya que requiere múltiples intervenciones para elongar el catéter atrial intracardíaco.Tiene como inconveniente las complicaciones de origen vascular. el ventrículo lateral es la ubicación proximal preferida. Comunica los ventrículos, através de la vena yugular, con la vena cava superior; se la denomina derivación “ventriculoauricular” porque comunica los ventrículos cerebrales con el sistema vascular: el extremo distal del catéter está ubicado en la región de la aurícula cardíaca derecha.
Es el tratamiento de elección si el paciente sufre anomalías abdominales (intervenciones abdominales extensas, peritonitis, obesidad patológica, en niños prematuros que padecieron enterocolitis necrotizante y pueden no tolerar una derivación VP, etc.)
C. la menor longitud de los catéteres genera menor presión distal y, por lo tanto, menor efecto de sifón que la derivación VP.
3. Derivación de Torkildsen: A. comunica el ventrículo con el espacio cisternal B. prácticamente no se utiliza C. sólo es eficaz en la hidrocefalia obstructiva adquirida, ya que en los pacientes que padecen hidrocefalia congénita frecuentemente no se desarrollan las vías subaracnoideas normales de reabsorción del LCR 4. otros sistemas de derivación que se colocaron en otros sitios de derivación distal (utilizadas en el pasado) o en pacientes en los que hubo problemas significativos en los sitios en que tradicionalmente se colocan las derivaciones (p. ej., peritonitis con una derivación VP, EBS con una derivación vascular): A. espacio pleural (derivación ventriculopleural): no es una primera opción, pero es una alternativa viable si no está disponible el peritoneo33. Existen riesgos de provocar un hidrotórax sintomático, lo que requiere la recolocación del extremo distal. Sólo se recomienda para pacientes > 7 años de edad B. vesícula biliar C. uretra o vejiga: se complica con desequilibrios electrolíticos a causa de la excreción en la orina 5. derivación lumboperitoneal (LP): A. sólo para tratar hidrocefalias comunicantes: seudotumor cerebral primario o fístula de LCR. Es de utilidad en las situaciones en las que los ventrículos son pequeños. Se le acusa en varias publicaciones de favorecer la migración transforaminal de las amígdalas cerebelosas. 6. B. en los pacientes mayores de 2 años de edad, se prefiere la inserción percutánea con una aguja Touhy derivación subdural o quística: desde la cavidad de un quiste aracnoideo o de un higroma subdural, generalmente, hacia el peritoneo.
Endoscopia
En la actualidad, es una técnica rutinaria para la hidrocefalia obstructiva. Sir Walter Dandy y otros empezaron a cauterizar o extirpar plexo coroideo por vía endoscópica a comienzos del siglo XX (Dandy 1913).
La ventriculostomía endoscópica representa una opción de tratamiento seguro en la hidrocefalia obstructiva por hemorragia intraventricular dando resultados similares al drenaje externo, pero con menos riesgo de infección y una muy baja tasa de necesidad de colocación de una derivación a posteriori. Sin embargo, realizar la técnica con un campo de visión borrosa y distorsionada de la anatomía ventricular supone un reto para cualquier neurocirujano endoscópico(Oertel 2009).
Hasta la llegada de las técnicas endoscópicas el tratamiento casi exclusivamente empleado ha sido el shunt ventricular desde el sistema ventricular al atrio inicialmente, y al peritoneo con posterioridad.
Es posible colocar un sistema de derivación para estabilizar el tamaño de la cabeza pero, a diferencia de lo que ocurre con la hidrocefalia máxima, no hay restitución del manto cerebral.
La mayoría de los pacientes se convierten en sujetos dependientes de estos sistemas valvulares de manera que la disfunción de los mismos se traduce en clínica de hipertensión intracraneal.
Indicaciones terapéuticas Las acumulaciones pequeñas (< 1-2 cm de espesor) y asintomáticas halladas en pacientes cuyas suturas craneales están cerradas pueden controlarse mediante un seguimiento imagenológico seriado. Los HSD son sintomáticos en = 40% de los casos (los síntomas frecuentemente se asemejan a los del mal funcionamiento valvular) y es necesario tratarlos. Se ha preconizado el tratamiento de los HSD en los niños cuyas suturas están aún abiertas como método de prevención de secuelas y de macrocefalia. Muchos autores recomiendan no tratar las lesiones asintomáticas sea cual fuere su aspecto, mientras que otros varían sus recomendaciones según diversos criterios, como el tamaño, el aspecto (crónico, agudo, mixto), etc.
Técnicas terapéuticas Se han descripto varias técnicas y la mayoría implica la evacuación del HSD mediante cualquiera de los métodos habituales (p. ej., agujeros de trepanación para las acumulaciones crónicas, craneotomía para las agudas) en combinación con: 1. una reducción del grado de derivación (es decir, establecer una presión menor en el espacio subdural que en el intraventricular, a fin de permitir que los ventrículos se reexpandan y se evite la formación de un nuevo HSD) A. en los casos dependientes de derivación 1. reemplazar la válvula por una de mayor presión 2. aumentar la presión en el caso en que la válvula sea de presión programable 3. utilizar el dispositivo Portnoy que tiene el sistema de apertura y cierre manejable desde el exterior. Es necesario asegurarse de que el personal de enfermería o los allegados del paciente estén instruidos para poder abrir el sistema ante una emergencia B. en los casos no dependientes de derivación 1. cualquiera de los métodos explicados bajo el punto “A”, o bien 2. desinstalación temporaria de la derivación C. inserción de un dispositivo antisifón 3. drenaje del espacio subdural hacia A. la cisterna magna B. el peritoneo, utilizando una válvula de baja presión (o sin válvula). Algunos autores recomiendan realizar un bombeo frecuente de la válvula subdural, que pueden llevar a cabo quienes cuiden al paciente El objetivo del tratamiento consiste en lograr un equilibrio delicado entre el hipodrenaje (que provoca síntomas de hidrocefalia activa) y el sobredrenaje (que propicia la reacumulación de un nuevo HSD). Después de la evacuación quirúrgica, el paciente debe ser movilizado lentamente para prevenir la recidiva del HSD.
Craneosinostosis, microcefalia y deformidades del cráneo Se han descrito varios cambios craneales en lactantes después de colocada una derivación: hiperostosis y endostosis de la base del cráneo y de la bóveda craneal, disminución del tamaño de la silla turca y de los orificios craneales y craneosinostosis. La deformidad craneal más frecuente es la dolicocefalia provocada por una sinostosis sagital. La microcefalia es responsable de = 6% de las deformidades craneales aparecidas después de colocada una derivación (aproximadamente la mitad tenía sinostosis sagital). Algunos de estos cambios fueron reversibles (excepto si hay sinostosis total) cuando hubo recidiva de la hipertensión intracraneal.
Independencia de la derivacion Aun no hay acuerdo acerca de cuando es posible decir que un paciente se ha independizado de la derivacion. Algunos consideran que esta independencia se logra con mas frecuencia en los casos en que la causa de la hidrocefalia es el bloqueo de las granulaciones aracnoideas (hidrocefalia comunicante), pero otros han demostrado que puede observarse en hidrocefalias de cualquier otra etiologia. En estos pacientes, es necesario realizar un seguimiento cuidadoso, puesto que algunos informes dan cuenta de muertes producidas hasta 5 años despues de la aparente independencia de la derivacion, en ocasiones, sin ningún preaviso.
Momento adecuado para retirar una derivacion desconectada o que no funciona Nota: una derivacion desconectada puede continuar funcionando con el flujo del LCR a traves de una via fibrosa subcutanea. Las recomendaciones respecto de si es conveniente reinstalar o retirar una derivacion desconectada o que no funciona son las siguientes: 1. si existen dudas, colocar una nueva derivacion
2.indicaciones para reinstalar una derivacion (en lugar de retirarla) A. derivaciones cuyo funcionamiento sea inconstante B. presencia de signos o sintomas de aumento de la PIC (vomitos, paralisis de la mirada hacia arriba, en ocasiones, cefalea sola. C. cambios en la funcion cognitiva, disminución campo de atención o cambios emocionales D. pacientes que presentan estenosis del acueducto o espina bífida: la mayoria es dependiente de la derivación.
3. debido a los riesgos asociados al retirar una derivación, solo debe realizarse una intervención quirúrgica con el único objetivo de retirarla si se sospecha que la derivacion está infectada. 4. es fundamental hacer un seguimiento cuidadoso de los pacientes que tienen una derivacion que no funciona mediante TC asociada a evaluaciones neurofisiologicas seriadas.
Ceguera por hidrocefalia La ceguera es una complicación poco frecuente de la hidrocefalia y del mal funcionamiento de una derivación. Entre las causas posibles se cuentan: 1. la oclusión de las arterias cerebrales posteriores (ACP) causada por una hernia transtentorial descendente 2. el papiledema crónico que lesiona el nervio óptico al nivel del disco (papila) 3. la dilatación del tercer ventrículo que comprime el quiasma óptico El mal funcionamiento de una derivación puede determinar ceguera, pero son más frecuentes las anomalías de la motilidad ocular o los defectos del campo visual. En una serie se hallaron 34 casos de niños que presentaron ceguera permanente atribuida al mal funcionamiento de la derivación y aumento concomitante de la PIC (estos autores basaron sus datos en un centro especializado en niños de visión defectuosa y, por ende, no estimaron la incidencia). En otra serie que incluyó a 100 pacientes que tenían una hernia tentorial (la mayoría provocada por un hematoma epidural o subdural agudo) comprobada mediante TC, se operó a 48 pacientes y sólo sobrevivieron > de 1 mes 19 de los 100 (todos pertenecían al grupo operado); 9 de los 100 presentaron infarto del lóbulo occipital (2 murieron, 3 quedaron en estado vegetativo y los 4 restantes padecieron discapacidades de moderadas a graves). Tipos de visión defectuosa Nueve de 14 pacientes presentaron ceguera pregeniculada (de la vía visual anterior), atrofia pronunciada (precoz) del nervio óptico y disminución del reflejo pupilar. Cinco de los 14 presentaron ceguera posgeniculada (cortical), reflejo pupilar normal y atrofia del nervio óptico mínima o ausente (o atrofia tardía). Pocos pacientes presentaron indicios de daño en ambos sitios. Ceguera cortical: causada por lesiones posteriores a los cuerpos geniculados externos (CGE), también puede observarse en las lesiones hipóxicas o en traumatismos. Ocasionalmente, está asociada al síndrome de Antón (negación de la deficiencia visual) y al fenómeno de Ridoch (percepción de los objetos en movimiento pero no de los estímulos estáticos). FlSIOPATOLOGÍA En pacientes que presentan infarto del lóbulo,occipital Los infartos del lóbulo occipital (ILO) en la distribución de las ACP se observan ya sea en ambos lados o en uno solo. Si son unilaterales, están asociados a algún otro daño de las vías ópticas retrogeniculadas. El mecanismo que está involucrado con mayor frecuencia es una hernia cerebral descendente que comprime las ACP. Si no, una hernia cerebelosa ascendente (p. ej., provocada por una punción ventricular en presencia de una masa ocupante en la fosa posterior), que puede distorsionar las ACP o alguna de sus ramas y provocar los mismos resultados.
Es más probable que se generen ILO si la PIC aumenta abruptamente (porque no permite que se produzcan desplazamientos compensatorios ni circulación colateral). Es frecuente que no esté afectada la mácula lútea. Las causas del ILO que se han relatado son: el edema postraumático, los tumores, los abscesos, los HSD, la hidrocefalia no tratada y el mal funcionamiento valvular. Los polos occipitales también son particularmente vulnerables a la hipoxia difusa, lo cual está confirmado por casos de ceguera cortical aparecidos después de un paro cardíaco. La hipotensión sumada al compromiso de la circulación de las ACP (causado por una hernia o por aumento de la PIC) puede incrementar el riesgo de ceguera posgeniculada. Tanto los traumatismos por golpe como por contragolpe pueden provocar ILO. A diferencia de lo que se observa en el infarto por oclusión de las ACP, en el traumatismo del lóbulo occipital puede estar afectada la mácula lútea“. En pacientes que presentan ceguera pregeniculada La PIC aumentada transmite presión a la retina —> estasis del flujo sanguíneo y trauma mecánico del quiasma óptico provocado por la dilatación del tercer ventrículo (se considera que este último es frecuentemente el principal responsable de la hemianopsia bitemporal, pero si no se lo controla, puede progresar hasta ceguera total). Por otra parte, si el paciente presenta hipotensión y anemia, es conveniente contemplar la posibilidad de que se trate de una neuropatía óptica isquémica. Signos y síntomas iniciales Estas manifestaciones frecuentemente pasan inadvertidas (el deterioro del estado mental y la juventud de muchos de estos pacientes dificultan la detección); el médico que realice la exploración debe perseverar para detectar hemianopsias homónimas en un paciente obnubilado. La ceguera pregeniculada está asociada con menor frecuencia que la posgeniculada a un sensorio deprimido (en esta última, son más probables la compresión directa y la afectación vascular del mesencéfalo).
Complicaciones
1. aquellas que pueden presentarse con cualquier tipo de derivación
A. obstrucción: es la causa más frecuente de mal funcionamiento del sistema.
• proximal: catéter ventricular (sitio más frecuente)
• mecanismo de la válvula
• distal: la incidencia oscila entre 12% y 34%. Se observa en el catéter peritoneal de la derivación VP (véase adelante) y en el catéter auricular de la derivación VA
B.desconexión en la unión o rotura en cualquier lugar
C. infección
D.erosión de la piel por el sistema de derivación. Generalmente, ocurre sólo en los pacientes debilitados (sobre todo, en los niños prematuros macrocefálicos que tienen el cuero cabelludo delgado a causa de la hidrocefalia crónica, que yacen sobre un lado de la cabeza debido a la deformidad craneana). Puede indicar también alergia a la silicona (véase adelante)
E.convulsiones (sólo con las derivaciones ventriculares): el riesgo de crisis convulsivas es de = 5,5% durante el primer año después de colocado el sistema de derivación, riesgo que se reduce a 1,1% después del tercer año36 (no significa que el sistema de derivación fue el causante de todas esas convulsiones). El riesgo de convulsiones es dudosamente mayor con los catéteres frontales que con los parietooccipitales
F. la derivación actúa como conducto de metástasis extraneurales de ciertos tumores (p. ej., meduloblastoma). Probablemente éste sea un riesgo relativamente bajo.
G.alergia a la silicona: muy poco frecuente (si es que se presenta). La manifestación puede ser similar a la de la infección de la derivación, que provoca alteración cutánea, solución de continuidad y granulomas fúngicos. Inicialmente, el LCR es estéril pero pueden presentarse infecciones con el paso del tiempo. Puede ser necesario fabricar un dispositivo sin silicona hecho a la medida (p. ej., de poliuretano)
2.derivación VP
A. la hernia inguinal tiene 17% de incidencia (muchos sistemas de derivación se insertan cuando el proceso inguinal se encuentra aún permeable)
B.es necesario alargar el catéter a medida que crece el niño: esto puede evitarse si se utiliza un catéter peritoneal largo C.obstrucción del catéter peritoneal es más probable en válvulas de apertura distal (“válvulas de hendidura”) a causa de una oclusión que provocan el epiplón o desechos atrapados de fibrina canalizados por el sistema de derivación.
-la formación de un quiste (o seudoquiste) peritoneal: por lo general, la formación de un quiste está asociada a una infección, pero también puede deberse a una reacción al talco de los guantes quirúrgicos. En raras ocasiones, puede llegar a ser necesario diferenciar una acumulación de LCR de la posibilidad de que se trate de orina, sobre todo en los pacientes que sufrieron una ruptura de la vejiga sobredistendida (p. ej., secundaria a una vejiga neurógena). Es posible aspirar el líquido por vía percutánea y analizar la concentración de urea y creatinina (que deberían estar ausentes en el LCR) - adherencias peritoneales graves: reduce la superficie de resorción del LCR
-mala posición de la punta del catéter:
• en el momento de la intervención: p. ej., en adiposidad preperitoneal
• el catéter distal puede llegar a salir de la cavidad peritoneal a causa del crecimiento
D. peritonitis provocada por una infección de la derivación
E. hidrocele
F. ascitis de LCR
G. migración de la punta del catéter
♦ que se adentre en el escroto
♦ que produzca la perforación de alguna viscera42: estómago, vejiga, etc. Es más frecuente que ocurra si se utilizan los antiguos tubos de derivación reforzados con resortes (Raimondi)
♦ que atraviese el diafragma
H. obstrucción intestinal (a diferencia de la perforación): muy poco frecuente
I. vólvulo
J. estrangulación intestinal: sólo se observó en pacientes en los que se intentó retirar el tubo peritoneal mediante tracción aplicada sobre el extremo cefálico de la incisión, lo que ocasionó la rotura del tubo, que dejó un segmento residual intrabdominal (en estas circunstancias, se recomienda realizar una exploración peritoneal inmediata)
K. sobredrenaje: es más probable que con la derivación VA. Algunos autores recomiendan la derivación LP para tratar la hidrocefalia comunicante
3. derivación VA:
A. es necesario alargar los tubos constantemente en los niños que están en etapa de crecimiento
B. mayor riesgo de infecciones, septicemia
C. posible reflujo de sangre hacia los ventrículos si la válvula no funciona correctamente (poco frecuente)
D. oclusión de la derivación por trombosis
E. complicaciones vasculares: perforación, tromboflebitis, microémbolos pulmonares que pueden causar hipertensión pulmonar47 (la incidencia es de = 0,3%).
4. derivación LP
A. en lo posible, no debe utilizarse en los niños que estén en etapa de crecimiento, salvo que el acceso ventricular resulte imposible (p. ej., en el síndrome de los ventrículos en hendidura) porque:
♦ la laminectomía practicada en niños causa escoliosis en 14%
♦ existen riesgos de provocar una hernia progresiva de las amígdalas cerebelosas (malformación de Chiari I) hasta en 70% de los casos
B. si se produce sobredrenaje, resulta más difícil controlarlo (se ha diseñado una válvula especial horizontal-vertical que aumenta la resistencia cuando el paciente está en posición vertical
C. resulta dificultoso acceder al extremo proximal para evaluar o comprobar la permeabilidad del sistema
D. irritación de las raíces nerviosas de la zona lumbar (radiculopatía)
E. filtración de LCR alrededor del catéter
F. resulta dificultoso regular la presión
G. disfunción bilateral de los pares VI y VII causada por sobredrenaje H. alta incidencia de aracnoiditis y adherencias
Dispositivos complementarios de los sistemas de derivación
1. filtro tumoral: se lo utiliza para prevenir siembras peritoneales o vasculares en presencia de tumores que puedan hacer metástasis a través del LCR (p. ej., los meduloblastomas, los tumores neuroectodérmicos primitivos y los ependimomas); las células tumorales pueden llegar a ocluir el filtro, en cuyo caso es necesario reemplazarlo; puede irradiarse el filtro tumoral para “esterilizarlo”. El riesgo de metástasis a través de la derivación es bajo.
3. la “válvula horizontal-vertical” (válvula H-V) se utiliza en las derivaciones LP para aumentar la presión de apertura de la válvula cuando el paciente está en posición vertical con el fin de evitar el sobredrenaje.
4. válvula “Sophy”: es una válvula de presión variable que es posible “programar” desde afuera mediante un imán potente 5. dispositivo de cierre (“on-off'): se lo utiliza para abrir o cerrar el sistema de la derivación mediante la manipulación externa del mecanismo (p. ej., dispositivo de Portnoy).
En cuanto a sistemas existen muchas en el mercado pero básicamente se pueden clasificar:
1.- Las de control de flujo
2.- De presión diferencial (3).
Problemas de las derivaciones Con cierta frecuencia, es necesario efectuar una evaluación neuroquirúrgica de los pacientes que tienen implantadas derivaciones de LCR y que presentan síntomas variados. Los “problemas” de las derivaciones generalmente consisten en una o más de las siguientes situaciones:
1. hipodrenaje
2. infecciones
3. sobredrenaje: síndrome de los ventrículos en hendidura, hematomas subdurales, etc.
4. convulsiones:
5. problemas vinculados al catéter distal
A. peritoneal:
B. auricular:
6. solución de continuidad cutánea de alguna de las partes del sistema: infecciones o alergia a la silicona
Punción de un sistema de derivación
Las indicaciones para realizar una punción de un sistema de derivación o de un dispositivo de acceso ventricular (p. ej., reservorio de Ommaya) son:
1. la obtención de muestras del LCR
A. para evaluar si hay una infección en el sistema de derivación
B. para realizar un análisis citológico: p. ej., en los casos de tumores neuroectodérmicos primitivos, con el fin de determinar si el LCR contiene células malignas
C. para evacuar sangre: p. ej., en el caso de una hemorragia intraventricular
2. la evaluación del funcionamiento del sistema
A. mediante la medición de las presiones
B. mediante estudios imagenológicos con contraste:
1. inyección proximal de contraste (yodado o de radiomarcadores)
2. inyección distal de contraste
3. la aplicación de una medida contemporizadora para permitir que vuelva a funcionar un sistema que tiene una oclusión distal
4. la inyección de medicación
A. antibióticos: como tratamiento de una infección o una ventriculitis
B. quimioterápicos (antineoplásicos)
5. la comunicación con catéteres colocados dentro de un quiste tumoral (no es una derivación genuina):
A. para hacer una evacuación periódica del líquido acumulado
B. para inyectar líquido radiactivo (generalmente, fósforo) a fin de realizar un tratamiento ablativo.
Es importante que todos los pacientes que padecen hidrocefalia y su familia estén informados de lo siguiente:
1. los signos y síntomas que indican un mal funcionamiento de la derivación
2. que no deben bombear la derivación a menos que así se les indique para un propósito específico
3. que debe instituirse profilaxis antibiótica en las siguientes situaciones (obligatoria en los casos de derivaciones vasculares; recomendada en otros tipos de derivación):
A. procedimientos odontológicos B. exploración instrumental de la vejiga: p. ej., cistoscopia. 4. que es necesario realizar evaluaciones periódicas en las cuales se estime la longitud del catéter distal, sobre todo en un niño en crecimiento.
HlPODRENAJE El índice de mal funcionamiento de las derivaciones es = 17% entre la población pediátrica durante el año posterior a la colocación. El mal funcionamiento puede deberse a: 1. un bloqueo (oclusión) A. causas posibles: 1. obstrucción por el plexo coroideo 2. acumulación de residuos proteínicos 3. sangre 4. células (inflamatorias o tumorales) 5. oclusión secundaria a una infección B. sitio del bloqueo 1. bloqueo del extremo ventricular (el más frecuente): por lo general, por el plexo coroideo, pero también puede deberse a adherencias gliales o sangre intraventricular.
2. bloqueo del sistema intermedio (válvulas, conectares, etc., los filtros tumorales pueden verse ocluidos por células tumorales, los dispositivos antisifón pueden cerrarse a causa de variaciones en la presión ejercida por el tejido subcutáneo suprayacente)
3. bloqueo del extremo distal
2. desconexión, acodamiento o rotura del sistema en cualquier punto: con el tiempo, los elastómeros de silicona que se utilizan en los catéteres se calcifican y pueden quebrarse, y al hacerse más rígidos y frágiles, provocan adherencias subcutáneas. La impregnación con bario puede acelerar este proceso. Los catéteres frecuentemente se rompen cerca de la clavícula, lo cual, según se presume, tiene su origen en la gran movilidad de la zona Signos y síntomas del hipodrenaje Los signos y síntomas son los mismos que los de la hidrocefalia activa: 1. síntomas de aumento agudo de la PIC A. cefalea B. náuseas y vómitos C. diplopía D. letargo E. ataxia F. lactantes: apnea, bradicardia; irritabilidad G. convulsiones: primera aparición, aumento de la frecuencia o dificultad para controlarlas 2. signos de aumento agudo de la PIC A. parálisis de la mirada hacia arriba (“signo del sol poniente”) B. parálisis del recto externo de uno o ambos ojos: falso signo de localización C. estrechamiento del campo visual o ceguera D. papiledema (poco frecuente antes de los 2 años de edad) E. lactantes: fontanela tensa y protuberante, ingurgitación de las venas del cuero cabelludo 3. edema en el trayecto de los catéteres: a causa del LCR que se escurre de alguno de los componentes de la derivación 4. cambios crónicos: antes de que se cierren las suturas, aumento del perímetro cefálico (entrecruzamiento de las curvas) Métodos para determinar el mal funcionamiento de una derivación 1. el objetivo de la anamnesis y la exploración física es determinar la presencia de los signos y síntomas mencionados; además, se debe establecer: A. el motivo por el cual se colocó la derivación (mielomeningocele, posmeningitis, etc.)
B. la fecha de la última revisión y el motivo por el cual se llevó a cabo
C. la presencia de accesorios en el sistema (p. ej., dispositivo antisifón, etc.)
D. en los niños: el perímetro cefálico. Transportar sobre un gráfico de curvas normales (utilizar el gráfico del paciente si está disponible) E. tensión de las fontanelas (si aún están abiertas): si la fontanela pulsa suavemente en forma sincrónica con las respiraciones, es un signo indicativo de normalidad; si por el contrario protruye y está tensa, es signo indicativo de una posible obstrucción; una fontanela deprimida puede ser normal o corresponder a sobredrenaje F. evaluación de la capacidad de bombeo de la válvula y de su relleno espontáneo: 1. precaución: puede agravar la obstrucción, sobre todo si la derivación está ocluida por el epéndimo en casos de sobredrenaje: discutido 2. dificultad para deprimirla: indica una oclusión distal 3. rellenado lento (en general, toda válvula debe rellenarse en 15-30 segundos): indica una oclusión proximal (ventricular) G. indicios de que ha escurrido LCR del sistema H. en los niños que sólo presentan vómitos, sobre todo aquellos que padecen parálisis cerebral y que tienen una gastrostomía, es necesario descartar reflujo gastroesofágico 2. exploración radiográfica A. estudios necesarios para evaluar la derivación (radiografías simples para visualizar todo el sistema: para las derivaciones VP, radiografías de cráneo AP y lateral + radiografía “baja” de tórax o radiografía abdominal) 1. descartar una desconexión o migración de la punta mediante radiografía en la que se visualice todo el sistema; nota: una derivación desconectada puede continuar funcionando por pasaje del LCR a través de un túnel fibroso subcutáneo; los siguientes elementos son radiotransparentes y pueden dar la imagen radiográfica de una desconexión:
a. la parte central de silástico de una válvula Holter
b. los conectores (en “Y” y en “T”, y también los rectos), sobre todo si son de plástico
c. los dispositivos antisifón
d. los filtros tumorales
2. deben esta disponibles las radiografías más recientes para compararlas en busca de soluciones de continuidad (es importante en los casos de derivaciones “complicadas” que tienen varios catéteres colocados en distintas cavidades ventriculares o quísticas, o que tienen dispositivos accesorios)
B. en los pacientes cuyas fontanelas están aún abiertas, la ecografía es un método óptimo de evaluación (sobre todo, si están disponibles ecografías previas)
C. la TC es necesaria para evaluar a los pacientes en quienes las fontanelas ya están cerradas; puede ser aconsejable en las derivaciones complicadas (p. ej., derivaciones de quistes)
D. RM: es demasiado costosa y lenta para efectuar la evaluación de rutina de una derivación y, además, no permite ver con claridad el sistema. No obstante, puede llegar a ser invalorable en los casos complicados (puede mostrar la reabsorción transependimaria del LCR, la existencia de loculaciones, etc.)
E. visualización directa del sistema (“shuntografía”) si quedan dudas sobre el funcionamiento de la derivación:
1. gammagrafía:
2. con contraste yodado: p. ej., iohexol (Omnipaque 180)
3. punción de la válvula de derivación: las indicaciones varían, pero generalmente se lleva a cabo si se contempla la posibilidad de efectuar una revisión quirúrgica o si existen fuertes sospechas de infección
4. exploración del sistema de derivación: en ocasiones, incluso después de realizar una evaluación completa, el único medio para comprobar o desestimar definitivamente el mal funcionamiento de alguno de los componentes de una derivación consiste en operar, aislar y someter a prueba cada parte del sistema por separado. Incluso si no existiesen sospechas de la presencia de infección, es necesario hacer un cultivo del LCR y de todo componente retirado.
Gammagrafía de la derivación (“shuntografía”)
También denominada “shuntogammagrafía/shuntograffa radioisotópica”. Procedimiento: afeitar y preparar la zona con polividona yodada. Con el paciente acostado en posición decúbito supino, efectuar la punción de la válvula insertando una aguja con aletas de 0,508 mm de diámetro externo (25 G) en el reservorio. A continuación, medir la presión y extraer 2-3 mi de LCR; enviar 1 mi de LCR para estudio bacteriológico. Inyectar el radioisótopo (p. ej., para una derivación VP de un adulto, utilizar 1 mCi de pertecneciato sólo o preferentemente quelado con DTPA (DTPA TC99m) (variación de uso: 0,5 mCi a 3 mCi) en 1 mi de solución salina) mientras se ocluye el extremo distal (comprimiendo la válvula o los acoples). Enjuagar la jeringa con LCR para facilitar la dilución del isótopo con el resto del LCR. En los pacientes que tienen colocados varios catéteres ventriculares, es necesario inyectar cada rama en forma independiente para verificar su permeabilidad. A continuación, hacer una gammagrafía del abdomen para descartar que el trazador no se haya inyectado directamente hacia el catéter distal. Luego obtener una gammagrafía de la cabeza para comprobar la entrada del radioisótopo en los ventrículos (determinación de la permeabilidad proximal). Se esperan 10 minutos y se hace nueva gammagrafía abdominal. Si no se comprueba flujo espontáneo hacia el abdomen, se hace sentar al paciente y se repite la gammagrafía al cabo de otros 10 minutos. Si aún no se visualiza el pasaje al abdomen, se procede a efectuar el bombeo manual de la válvula y se obtiene un nuevo barrido de la zona. Si no pasa, seguramente esté bloqueado. En cualquiera de las circunstancias, cuando hay pasaje, es necesario verificar la dispersión del trazador en el abdomen para descartar la existencia de formaciones seudoquísticas peritoneales alrededor del extremo del catéter. Infección de la derivación
“Sobredrenaje” Posibles complicaciones por sobredrenaje 1. ventrículos en hendidura: incluido el síndrome de los ventrículos en hendidura 2. hipotensión intracraneal: 3. hematomas subdurales: 4. craneosinostosis y microcefalia: muy discutidos 5. estenosis u oclusión del acueducto de Silvio Entre 10% y 12% de los pacientes que tienen colocadas derivaciones ventriculares durante un tiempo prolongado padecen alguno de los problemas mencionados después de 6,5 años de la colocación. Algunos especialistas consideran que sería posible reducir los problemas vinculados al sobredrenaje utilizando derivaciones LP para tratar la hidrocefalia comunicante y reservando las ventriculares para tratar la hidrocefalia obstructiva. Es probable que las derivaciones VP sobredrenen más que las LP debido a que los catéteres de estos sistemas tiene una mayor longitud —> mayor efecto de sifonaje.
Hipotensión intracraneal
También denominada “síndrome de la PIC baja”, es muy poco frecuente y sus síntomas son similares a los de la cefalea por punción lumbar (de naturaleza postural, que se alivia con el reposo). Si bien no está obligatoriamente asociada a los síntomas que se mencionan a continuación, estos pueden presentarse: náuseas y vómitos, letargo o signos neurológicos (p. ej., diplopía, parálisis de la mirada hacia arriba). En ocasiones, los síntomas son similares a los causados por un aumento de la PIC, con la excepción de que mejoran con el reposo en cama. Los efectos agudos que pueden suscitarse son: taquicardia, desmayo, déficit del tronco encefálico a causa del desplazamiento rostral del contenido intracraneal por disminución de la PIC. La causa de la hipotensión intracraneal es el efecto de sifón provocado por la columna de LCR que se forma en el tubo de la derivación cuando el paciente está de pie. Los ventrículos pueden estar colapsados (como en el síndrome del ventrículo en hendidura (SVH)) o pueden tener aspecto normal. En algunas ocasiones, es necesario documentar una caída abrupta de la PIC al pasar el paciente de la posición supina a la erecta para diagnosticar esta afección. Estos pacientes pueden presentar también oclusión de la derivación, lo que dificulta aún más diferenciarla del SVH.
Si los síntomas son de instalación reciente, el tratamiento de elección es la colocación de un sistema antisifón. Por el contrario, los pacientes en los que el sobredrenaje es de larga data pueden no tolerar los intentos de llevar la presión intraventricular a niveles normales.
La cefalea postural causada por hipotensión intracraneal (sobredrenaje real) se resuelve espontáneamente; sin embargo, si los síntomas persisten al cabo de mantener 3 días de reposo absoluto, con analgésicos y con una faja abdominal bien ceñida, debe controlarse que la válvula tenga la presión de cierre adecuada. Si la válvula instalada es de presión baja será necesario reemplazarla por una de mayor presión. Si no es de presión baja, puede ser necesario colocar un dispositivo antisifón (DAS) (que, por sí solo, también aumenta la resistencia del sistema) como único cambio o junto con una válvula de mayor presión.
Ventrículos en hendidura (Slit ventricle syndrome).
Hematomas subdurales
Los hematomas subdurales (HSD) pueden estar ocasionados por un colapso del cerebro acompañado de desgarro de las venas puente. En la época en que no existía la TC, la incidencia de la formación de HSD después de la colocación de una derivación se estimaba en = 1,2%, valor probablemente subestimado. Algunas publicaciones más recientes informan de una incidencia que va de 4% a 23% entre los adultos y de 2,8% a 5,4% entre los niños; es mayor en los casos de hidrocefalias normotensivas (de 20% a 46%) que en los de “hidrocefalias hipertensivas” (de 0,4% a 5%). El riesgo de formación de un HSD es mayor en cuadros prolongados de hidrocefalia que tienen un cráneo grande y escaso manto cerebral (desproporción craneocerebral), lo cual es frecuente en los niños que presentan cabeza grande (macrocrania) y ventrículos dilatados en la primera consulta. Estos pacientes tienen un “equilibrio muy delicado entre la presión subdural y la intraventricular”. El HSD también puede complicar una derivación en los ancianos que presentan atrofia cerebral importante. La formación de un HSD también puede verse facilitada por los episodios de presión intraventricular negativa que provoca el efecto de sifón. Por el contrario, existe un bajo riesgo de que se formen hematomas epidurales como complicación de una derivación de LCR. Características de las acumulaciones líquidas: las acumulaciones de líquido pueden estar del mismo lado que la derivación en 32% de los casos, en el lado opuesto en 21% y pueden ser bilaterales en 47%. En el momento de su diagnóstico, los HSD generalmente se encuentran en estado evolutivo que va de subagudo a crónico, y los ventrículos que estaban anteriormente dilatados están colapsados. Sólo en 1 de 19 casos se encontró líquido incoloro. En todos los casos, el contenido proteínico fue elevado en comparación con el del LCR.
Pronóstico
Es frecuente que mejore la ceguera cortical provocada por una anoxia difusa (en ocasiones, hasta se normaliza); esta mejoría se produce, por lo general, lentamente (se ha informado desde meses hasta años; generalmente, el proceso lleva varios meses). Muchos informes de casos de ceguera de aparición posterior a una disfunción valvular pertenecen a la época anterior a la TC y, por ende, la presencia o la extensión del infarto del lóbulo occipital no pudo establecerse con certeza. Si bien existen algunas comunicaciones que tienen pronósticos optimistas, también están las que describen casos de ceguera permanente y de defectos visuales acentuados; hasta el presente, no se ha identificado ningún signo pronóstico que sea fiable. Al igual que en los infartos producidos en cualquier otra parte del cuerpo, los pacientes jóvenes tienen un pronóstico más auspicioso, pero los infartos extensos de la calcarina comprobados mediante TC probablemente sean incompatibles con una recuperación visual significativa.
Hidrocefalia y embarazo Las pacientes que tienen instalado un sistema de derivación de LCR pueden quedar embarazadas; existen informes de al menos 4 casos que presentaron hidrocefalia durante el embarazo y fue necesario colocarles una derivación. Con las derivaciones VP, los problemas del catéter distal pueden ser mayores durante el embarazo. A continuación, proporcionamos algunas sugerencias modificadas, que fueron tomadas de Wisoff y cois. respecto de la actitud diagnóstico-terapéutica que debe tomarse frente a estas pacientes.
Actitud diagnóstico-terapéutica antes de la concepción 1. evaluación: A. del funcionamiento de la derivación: realizar RM o TC antes de la concepción para tomar los estudios como referencia. Es necesario evaluar la permeabilidad de la derivación si hay sospechas de una disfunción. Las pacientes que tienen ventrículos en hendidura pueden tener reducida la distensibilidad cerebral y pueden volverse sintomáticas con cambios muy pequeños de volumen B. de los fármacos que esté utilizando la paciente, sobre todo, si está en tratamiento anticonvulsivo 2. asesoramiento: A. asesoramiento genético: si la hidrocefalia se debe a una ACTN, entonces la probabilidad de que el bebé tenga una ACTN es de 2% a 3% B. otras recomendaciones: administrar vitaminas prenatales y evitar los fármacos teratógenos y el calor excesivo (p. e)., jacuzzi).
Actitud diagnóstico-terapéutica durante el embarazo 1. observación minuciosa en busca de signos de aumento de la PIC: cefalea, náuseas y vómitos, letargo, ataxia, convulsiones, etc. Precaución: estos signos pueden ser similares a los de una preeclampsia (que también es necesario descartar). De estas pacientes, 58% presenta signos de PIC aumentada, que puede deberse a: A. descompensación de una disfunción parcial de la derivación B. mal funcionamiento de todo el sistema de derivación C. algunos signos de PIC aumentada que se manifiestan a pesar de que la derivación funcione adecuadamente pueden deberse a hiperhidratación cerebral o a congestión venosa D. formación de un tumor cerebral durante el embarazo 2. es necesario obtener TC o RM de todas las pacientes que presenten síntomas de PIC aumentada A si no hay cambios desde el estudio realizado antes de la concepción, punzar la derivación para medir la PIC y realizar un cultivo de LCR. También es aconsejable contemplar la realización de una gammagrafía de la derivación (“shuntografía”) B si todos los estudios arrojan resultados negativos, es probable que los síntomas se deban a los cambios fisiológicos. El tratamiento en estos casos es reposo absoluto, restricción hídrica y, en los casos graves, corticoides o diuréticos (ambos o por separado). Si los síntomas no ceden, se recomienda efectuar un parto adelantado en cuanto pueda asegurarse la madurez pulmonar del feto (administrar profilaxis antibiótica durante las 48 horas anteriores al parto) C. si los ventrículos se agrandaron o se comprueba una disfunción valvular en la evaluación, es necesario revisar su funcionamiento 1. en los primeros dos trimestres: se prefiere una derivación VP, que las pacientes toleran sin problemas (no utilizar el método del trocar peritoneal después del primer trimestre) 2. en el tercer trimestre: se utiliza una derivación VA o ventriculopleural para evitar el traumatismo uterino o la inducción del parto.
Actitud diagnóstico-terapéutica durante el parto
1. se recomienda administrar profilaxis antibiótica durante el trabajo de parto y el parto para reducir la incidencia de infecciones de la derivación. Dado que, durante el trabajo de parto, los patógenos más frecuentes son los coliformes, Wisoff y cois, recomiendan administrar 2 g de ampicilina i. v. cada 6 horas y 1,5 mg/kg de gentamicina i. v. cada 8 horas durante el trabajo de parto y x 48 horas después del parto120 2. en las pacientes que no presentan síntomas: se lleva a cabo el parto vaginal si es factible desde el punto de vista obstétrico (es menor el riesgo de que se formen adherencias o que se infecte el catéter distal). Se prefiere un período expulsivo corto puesto que el aumento de la presión del LCR en este período probablemente sea mayor que en cualquier otra maniobra de Valsalva. 3. en las pacientes que se vuelven sintomáticas cuando el embarazo está cercano al término o durante el trabajo de parto, después de estabilizar a la paciente, se realiza una cesárea con anestesia general (las anestesias epidurales están contraindicadas en presencia de PIC aumentada) al tiempo que se moni torea cuidadosamente el aporte líquido (p. ej., mediante un catéter central) y, en los casos graves, se administran corticoides y diuréticos.
Bibliografía
Dandy WE, Blackfan KD: An experimental and clinical study on internal hydrocephalus. JAMA 61:2216–2217, 1913.
Joachim M. K. Oertel,, Yvonne Mondorf, Joerg Baldauf, Henry W. S. Schroeder, Michael R. Gaab.Endoscopic third ventriculostomy for obstructive hydrocephalus due to intracranial hemorrhage with intraventricular extension.J Neurosurg. 2009 Dec 28.