Astrocitoma
Epidemiología
Constituyen el 25-30 por ciento de los gliomas.
La célula predominante en estos tumores deriva de los astrocitos y constituyen aproximadamente un 80% de los tumores neuroepiteliales.
La relación astrocitoma intracraneal: astrocitoma medular es 10:1.
Clasificación
Astrocitoma difuso IDH mutado
Astrocitoma gemistocítico IDH mutado
Astrocitoma difuso IDH nativo
Astrocitoma difuso NOS
Astrocitoma anaplásico IDH mutado
Astrocitoma anaplásico IDH nativo
Astrocitoma anaplásico NOS
Oligoastrocitoma NOS
Oligoastrocitoma anaplásico NOS
Astrocitoma pilocítico
Astrocitoma pilomixoide
Astrocitoma de células gigantes subependimario
Xantoastrocitoma pleomórfico
Xantoastrocitoma pleomórfico anaplásico
Astrocitoma y ganglioglioma displásico infantil
Según la OMS
Grado I-OMS: Astrocitoma pilocítico
Grado II-OMS: Astrocitoma de bajo grado difuso
Grado III-OMS: Astrocitoma anaplásico
Grado IV-OMS: Glioblastoma multiforme
Clasificación histológica WHO 2007
- Astrocitomas
- Astrocitomas difusos
- Fibrilares
- Protoplasmicos
- Lesiones más circunscritas
- Astrocitoma pilocítico
- Astrocitoma pilomixoide
- Xantoastrocitoma pleomórfico
- Astrocitoma subependimario de células gigantes
Pronóstico
Las lesiones más circunscritas tienen mejor pronóstico.
El criterio histológico que afecta al pronóstico inclye: celularidad, presencia de células gigantes, necrosis y pseudopalisada (Bigner 1998).
Además de la histología juegan un papel fundamental, la edad, extensión tumoral y localización.
El sistema de Kernohan ya no se utiliza
Los 2 sistemas usados son:
1.En 1993, la Organización Mundial de la Salud (OMS) estableció los criterios para clasificar los astrocitomas en cuatro grados basados en sus características histológicas:
Grado I: Astrocitoma de bajo grado, poco frecuentes que cursan con un excelente pronóstico después de su extirpación, aparecen en niños más que en adultos.
Grado II: Astrocitoma propiamente dicho, que junto con el grado I constituyen aproximadamente un 6% de todos los tumores de cerebro reportados.
Grado III: Astrocitoma anaplásico, un tumor difuso, infiltrante caracterizado por anaplasia dispersa y elevado potencial proliferativo, por lo general aparecen de un astrocitoma de bajo grado aunque pueden ser diagnosticados sin un precursor. Igualmente, tienen un potencial intrínseco de progresar a un glioblastoma maligno. Son tumores predominantes en personas de raza blanca y en la quinta década de vida.
Grado IV: Glioblastoma multiforme, el más frecuente con una incidencia máxima a los 65 años aproximadamente y crece principalmente en los hemisferios cerebrales y tiende a ser el tumor más agesivo, clínicamente, entre los astrocitomas. La sobrevida de pacientes con glioblastoma multiforme se extiende a unos 12 meses con tratamiento quirúrgico agresivo junto con radio y quimioterapia. La sobrevida de 5 años no suele subir del 3%. Es posible que un astrocitoma que inicialmente fue de bajo grado recurra a una forma más agresiva y extensa.
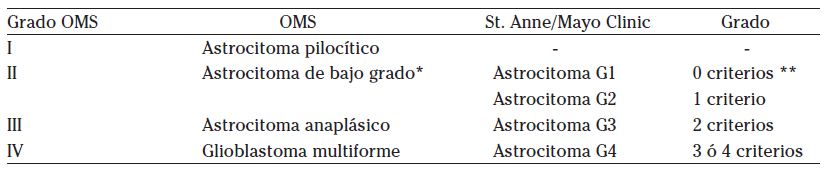
2. Criterios St.Anne/Mayo
Basado en los indicadores histológicos de anaplasia tal y como han sido definidos por Daumas-Duport:
atipia nuclear, el número de mitosis, la proliferación vascular y la presencia de necrosis.
Estos criterios sirven para clasificar a los astrocitomas en cuatro grupos de creciente agresividad histológica y peor pronóstico, en la clasificación de St. Anne/Mayo.
Relación Glioblastoma/atrocitoma anaplásico/astrocitoma de bajo grado 5/3/2.
Astrocitoma de bajo grado (WHO II)
Astrocitoma maligno (WHO III y IV).
Bibliografía
Bigner, Darell D., Roger E. McLendon, y Janet M. Bruner. 1998. Russell & Rubinstein's Pathology of Tumors of the Nervous System. 6º ed. A Hodder Arnold Publication, Junio 15.