Glioblastoma
Tumor neuroepitelial, astrocítico.
Es el tipo más común y agresivo de glioma maligno, caracterizado por su alta invasión del tejido cerebral circundante, y una de las formas más agresivas de cáncer humano (Wen y col., 2008).
Presenta dos variedades: el glioblastoma de células gigantes y el gliosarcoma.
Historia
En la primera mitad del siglo XIX el glioblastoma se consideraba de origen mesenquimal y por tanto se definió con el término de sarcoma.
En 1863, Rudolf Virchow demostró su origen glial.
F.B. Mallory, en una memoria de 1914, propuso el término glioblastoma multiforme.
Sin embargo, hubo que esperar hasta 1925 para tener una descripción completa de la neoplasia, por parte de J.H. Globus e I. Strass. En esta época, la denominación más común del tumor era espongioblastoma multiforme.
En 1926, una publicación de P. Bailey y H. Cushing volvió a proponer, con éxito, la expresión de Mallory.
La clasificación OMS de 2000 de los tumores del sistema nervioso fija finalmente el nombre de glioblastoma.
Epidemiología
Los glioblastomas multiformes son los tumores cerebrales primarios mas frecuentes.
En el 2011 la incidencia es de aproximadamente 10.000 habitantes de EE.UU cada año.
Se presenta con una frecuencia de 2 a 3 casos nuevos anuales por cada 100.000 habitantes, en la mayor parte de los países europeos y EE.UU (Jemal y col., 2010).
Los glioblastomas son poco frecuentes en los niños (0,6-7,9 % de todos los glioblastomas), y el pronóstico es mejor que la de los glioblastomas observados en adultos (Márquez-Rivas 2010; Khalatbari y col., 2011).
La incidencia en el noroeste de Grecia fue mayor en comparación con los datos de otros estudios realizados en Europa, Asia y EE.UU (Gousias y col., 2009).
En un trabajo publicado sobre la población de Gironde en Francia, se ha observado un incremento desde 1980. La mejora en las herramientas de diagnóstico tales como una tomografía computarizada y resonancia magnética, los cambios observados en las clasificaciones histológicas, y los ajustes en las prácticas de neurocirugía han contribuido sustancialmente a este aumento. Por otra parte, el envejecimiento de la población y la creciente incidencia del glioblastoma en pacientes mayores de 60 años de edad son explicaciones adicionales.
En esta región de Francia, se ha establecido un registro especializado, siendo la incidencia anual del glioblastoma 4.96/100, 000.
Se observan amplias variaciones geográficas, posiblemente vinculadas con el origen étnico. Sin embargo, el papel de los factores intrínsecos y / o extrínsecos no se pueden descartar. Comparar los datos entre los registros es difícil y requiere, herramientas de diagnóstico.
El origen étnico, edad, sexo, síndromes hereditarios, algunos polimorfismos constitutivos, y la irradiación del cerebro son importantes factores de riesgo.
Otros factores de riesgo son discordantes o no se confirmaron debido a las limitaciones metodológicas.
Los estudios futuros que combinen polimorfismos constitutivos y la evaluación de la exposición son susceptibles de proporcionar datos consistentes e importantes que mejorarán nuestro conocimiento de la epidemiología del glioblastoma (Baldi y col., 2010).
Clasificación
Glioblastoma IDH nativo
Glioblastoma de células gigantes
Glioblastoma epitelioide
Glioblastoma IDH mutado
Glioblastoma NOS
Subtipos
Proneural
Neural
Mesenquimal
Clásico
Un subtipo, se caracteriza por la amplificación frecuente o mutaciones en el receptor del factor de crecimiento epidérmico del protooncogen (EGFR)
Otro subtipo, denominado proneural, alberga mutaciones frecuentes en p53, crecimiento derivado de plaquetas receptor del factor A e isocitrato deshidrogenasa.
Un tercer tipo, denominado mesenquimal, se caracteriza por mutaciones frecuentes en la neurofibromatosis gen tipo 1 (NF-1).
Los estudios realizados por Phillips y Verhaak demostraron una mayor supervivencia global en pacientes con glioblastoma proneural en relación con otros subtipos moleculares (Phillips y col., 2006; Verhaak y col., 2010).
Según su desarrollo
Glioblastomas primarios o de novo, que se desarrollan más rápidamente, con una historia clínica de corta duración.
Glioblastomas secundarios, desarrollados mediante progresión tumoral a partir de astrocitomas de bajo grado (grado II de la OMS), o anaplásicos (grado III de la OMS).
Existe una evidencia creciente de que estos subtipos de glioblastomas constituyen dos entidades clínicas diferentes, que se manifiestan en pacientes de edad diferente y se desarrollan mediante rutas genéticas distintas.
Los glioblastomas primarios se presentan en pacientes de mayor edad y se caracterizan por la presentación de amplificación/sobreexpresión de EGFR (receptor del factor de crecimiento epidérmico), hiperactivación PI3K , mutaciones de PTEN, deleciones de p16 o sobreexpresión de MDM2, mientras que los glioblastomas secundarios se presentan en pacientes más jóvenes y contienen mutaciones de p53 como característica genética preponderante, aunque no exclusiva.
Grado de Kernohan
Características radiológicas
I TC: hipodensidad RM: señal anómala no se observa efecto de masa ni refuerzo
II TC: hipodensidad RM: señal anómala se observa efecto de masa pero no refuerzo
III: refuerzo complejo
IV:necrosis (refuerzo en anillo)
La clasificación de los gliomas mediante TC o RM es imprecisa, pero es de utilidad como evaluación preliminar.
Esta clasificación no es aplicable a los pacientes pediátricos.
La mayoría de los gliomas de bajo grado no se observan con refuerzo ni en la TC ni en la RM (aunque algunos autores opinan que hasta 40% presenta refuerzo, en cuyo caso probablemente tengan peor pronóstico).
Por lo general, son hipodensos en la TC. La mayoría son hipointensos en las imágenes T1 de RM y, en T2, presentan cambios que exceden el volumen del tumor.
Algunos gliomas malignos se observan sin refuerzo. Refuerzo en anillo de los glioblastomas multiformes: el centro de hipodensidad que se observa en la TC representa la necrosis. El anillo de refuerzo que lo rodea es el tumor celular, pero también se han hallado células tumorales hasta una distancia de 15 mm del anillo.
Localización
Los datos de tres registros de cáncer demuestran un aumento de la incidencia de glioblastomas en el lóbulo frontal, lóbulo temporal, y el cerebelo, y una reducción de la incidencia en otras regiones del cerebro. Aunque esto puede representar un sesgo, la causa de estas tendencias observadas es desconocida (Zada y col., 2011).
Los glioblastomas multiformes de ubicación infratentorial son infrecuentes y, a menudo representan una diseminación subaracnoidea de un tumor supratentorial, lo cual se utiliza como justificación para la radioterapia holocraneal.
Etiología
Los estudios llevados a cabo desde los 1980s sugieren que los glioblastomas, al igual que otros tipos de cáncer, surgen como acumulación de alteraciones genéticas.
Estas alteraciones pueden tomar la forma de modificaciones epigenéticas, mutaciones puntuales, translocaciones, ampliaciones o supresiones y modificar las funciones de los genes de una manera que desregulan las vías de señalización celular que conducen al fenotipo del cáncer (Stratton y col., 2009).
Se han descrito multitud de factores etiológicos como la exposición a corrientes eléctricas, el uso de teléfonos móviles pero de todos ellos el único factor etiológico descrito como causante de un glioma de alto grado es la exposición crónica a derivados petroquímicos.
Herencia
Si bien existen síndromes en los que estos tumores presentan familiaridad, estas situaciones (neurofibromatosis, síndrome de Turcot, síndrome de Li-Fraumeni, etc.) son muy poco frecuentes y normalmente conocidas por la familia antes de que se desarrolle un tumor en un miembro familiar.
Etiopatogenia
El desarrollo de glioblastomas podría estar ligado a amplificación de EGFR (cromosoma 7) y ERBB2 (cromosoma 17), además de a otros loci, mientras que las deleciones podrían asociarse a pérdida de función de los genes supresores de tumores RB (cromosoma 13), pl6 (cromosoma 9), PTEN y DMBT1 (cromosoma 10). Por el contrario, p53, en el cromosoma 17, no se mostró afectado.
La diversidad y la cantidad de las alteraciones moleculares presentes en glioblastomas probablemente sea el motivo por el que todavía no se han encontrado fármacos efectivos para combatirlos.
En la actualidad, con la aparición de nuevas técnicas de biología molecular, se puede intentar individualizar y clasificar a los pacientes en función de su expresión génica.
Esto abre una ventana esperanzadora a la aparición de nuevos fármacos que tengan como diana exclusiva a los genes y/o proteínas alterados de las células tumorales en función de su patrón de expresión génica individualizado para cada tumor (Franco-Hernández y col., 2007).
El desarrollo de glioblastomas podría estar ligado a amplificación de EGFR (cromosoma 7) y ERBB2 (cromosoma 17), además de a otros loci, mientras que las deleciones podrían asociarse a pérdida de función de los genes supresores de tumores RB (cromosoma 13), pl6 (cromosoma 9), PTEN y DMBT1 (cromosoma 10).
Por el contrario, p53, en el cromosoma 17, no se mostró afectado.
Muestran una hiperactivación de la vía PI3K-Akt, una cascada de señalización pro-tumorigénica que contribuye a la patogenia.
En resumen, se distinguen dos tipos de alteraciones:
la activación de factores oncogénicos:
EGF/R (Epidermal Growth Factor/Receptor, Factor de crecimiento epidérmico)
MDM2 (la oncoproteína Mouse Double Minute 2 promueve la supervivencia celular y la progresión del ciclo celular mediante la inhibición del supresor tumoral TP5357 )
PDGF/R (Platelet-Derived Growth Factor/Receptor, Factor de crecimiento derivado de plaquetas) la desactivación de factores oncosupresores:
10p, 10q, 19q (Cromosomas)
DCC (Deleted in Colorectal Cancer tumor suppressor gene, Gen con deleción en el cáncer colorrectal)
p16 (Tumor suppressor gene/protein, Antígeno supresor tumoral)
TP53 (Tumor suppressor gene/protein, Antígeno supresor tumoral)
PTEN (Phosphatase and TENsin homolog es un supresor tumoral que controla el crecimiento, la proliferación y la supervivencia celular. De su mutación o inhibición puede desencadenarse la aparición de tumores, por ejemplo, de próstata, mama, colon y cerebro.
RB (RetinoBlastoma tumor suppressor gene, Proteína del retinoblastoma)
Anatomía patológica
Es un tumor de rápido crecimiento, compuesto por una mezcla heterogénea de células tumorales astrocitarias pobremente diferenciadas, con pleomorfismo, necrosis, proliferación vascular y frecuentes mitosis.
Los hallazgos histológicos asociados a estos tumores son (es posible que no todos estén presentes; esta lista no sigue ninguno de los sistemas convencionales de clasificación ya mencionados):
• neovascularización con proliferación endotelial
• zonas de necrosis
• células en seudoempalizada que rodean las áreas de necrosis
Sobreexpresa los receptores α2 (IL-13Rα2), de la interleucina 13, un receptor de tumor restringido que no está presente en el cerebro normal (Nguyen y col., 2011).
Características anatomopatológicas
Se observan astrocitos gemistocíticos sólo en los astrocitomas gemistocíticos y en los glioblastomas multiformes.
La tinción para detectar la proteína acida fibrilar de la neuroglía es positiva en la mayoría de los astrocitomas (sin embargo, es probable que no sea positiva en algunos gliomas indiferenciados y en los astrocitomas gemistocíticos, porque es necesario que haya astrocitos fibrilares para que el resultado sea positivo).
Los gliomas pueden contener una zona de necrosis quística central, pero también pueden estar asociados a quistes, incluso sin necrosis.
Cuando se aspira líquido de estos quistes, es posible diferenciarlo del LCR porque, por lo general, es xantocrómico y, con frecuencia, se coagula una vez extraído (a diferencia de, p. ej., el líquido extraído de un higroma subdural crónico). Si bien los quistes pueden estar asociados a gliomas malignos, se asocian con mayor frecuencia a los astrocitomas pilocíticos.
Los gliomas de alto grado se clasifican en grado tres y cuatro y según Kernohan el grado 3 presenta atipias celulares mitosis y proliferación endotelial vascular.
El grado 4 presentaría además necrosis.
Según Daumas-Dauport el astrocitoma anaplásico presenta dos de estas características y el glioblastoma multiforme tres o cuatro de estos criterios.
Alteraciones Genéticas
En el desarrollo están implicados numerosos genes. Los estudios de pérdida de heterozigosidad (LOH) constituyen el método más ampliamente usado, desde el punto de vista molecular, para determinar la pérdida de material genético
Las alteraciones genéticas y epigenéticas frecuentes son la amplificación de EGFR (51,5%), la mutación del gen TP53 (33,8%), pérdida de CDKN2A (32,4%), pérdida de TP53 (16,2%), la metilación del promotor MGMT (33,8%) y la mutación IDH1 (5,9 %) (Motomura et al. 2011)
Pérdida de heterozigosidad (LOH) del cromosoma 10.
Alteraciones de la vía TP53/MDM2/P14arf
Alteraciones de la vía p16ink4/RB1/CDK4
Factores de crecimiento y angiogénicos sobrexpresados
Fisiopatología
Los gliomas pueden diseminarse de los siguientes modos (nota: < 10% de los gliomas recidivantes aparecen alejados del lugar afectado originalmente
1. a través de la sustancia blanca
A. cuerpo calloso (CC)
1. a través de la rodilla o del cuerpo del CC -» compromiso bilateral del lóbulo frontal (“glioma en alas de mariposa”)
2. a través del rodete del CC —> compromiso bilateral del lóbulo parietal
B.pedúnculos cerebrales —> compromiso del mesencéfalo
C. cápsula interna —> los tumores alojados en los núcleos básales invaden el centro semioval
D.fascículo uncinado —> tumores simultáneos de los lóbulos frontal y temporal
E.comisura intertalámica —> gliomas talámicos bilaterales
2. por vía del LCR (siembra subaracnoidea): los gliomas de alto grado provocan siembras meníngeas y ventriculares con una frecuencia de 10%-25%
3.es infrecuente que la diseminación se produzca por vía circulatoria general.
Es uno de los tumores mas vascularizados ya que expresa VEGF y factores proangiogénicos.
Clínica
La clínica de estos tumores viene dictada por la compresión que produce, la destrucción parenquimatosa , el bloqueo de la circulación del líquido cefaloraquídeo así como la compresión vascular. Se caracteriza por el déficit neurológico progresivo. Un 50% presentan cefaleas de carácter matutino acompañado de náuseas y vómitos. Un 30% de los casos presenta una crisis epiléptica. Pueden haber alteraciones psiquiátricas en el sentido de cambios de carácter. Compresión de Pares craneales. Deterioro brusco del nivel de conciencia por hemorragias edema peritumoral masivo, hidrocefalia por obstrucción del líquido cefaloraquídeo. Puede haber también síndrome de isquemia transitorias por obstrucción de vasos.
Diagnóstico
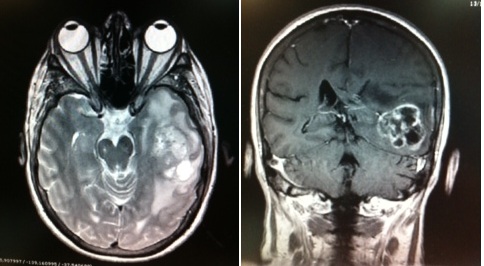
En las imágenes de TC y RM se muestra como una lesión heterogénea, de contorno irregular, que capta contraste en anillo y con un área central necrótica.
Se debe realizar Resonancia nuclear magnética con contraste.
Los hallazgos se pueden dividir en cuatro grados de Kernohan:
El grado tres que se caracteriza por captación de contraste sin efecto masa y el cuarto grado por captación de contraste y efecto masa.
En RM tras la administración de Gadolinio endovenoso se evidencia un realce heterogéneo y periférico, con componente quístico necrótico, generalmente la lesión se acompaña de alteración de la señal de morfología digitiforme de la sustancia blanca adyacente.
Diagnóstico Diferencial
El diagnóstico diferencial habrá que realizarlo con todos las lesiones que captan contraste en anillo como son la metástasis, absceso cerebral pero también con infarto cerebral y linfoma.
Tratamiento
Ver Exéresis de glioblastoma multiforme.
Un estudio publicado en julio de 2011 en el Journal of Neurosurgery, los autores encontraron una ventaja de supervivencia significativa en resecciones subtotales con una extensión de resección de tan sólo el 78%, con una mejora gradual en la supervivencia a partir de allí e incluso en el rango del 95% -100% (Sanai y col., 2011).
En el estudio retrospectivo de Lacroix y col., sólo las resecciones del 98% o más del volumen inicial del tumor se asociaron con una supervivencia prolongada (Lacroix y col., 2001).
En el estudio aleatorizado controlado con placebo multicéntrico de fase III, sobre cirugía guiada por fluorescencia con ácido 5-aminolevulínico (5-ALA) en el glioma maligno, la radicalidad quirúrgica fue aún más estricta utilizando valores absolutos para la estimación del volumen del tumor residual. Concretamente cualquier volumen mayor de 0,175 cm3 en una RM postoperatoria temprana (realizada dentro de 3 días después de la cirugía) fue clasificado como tumor residual (Pichlmeier y col., 2008).
Es importante tener en cuenta que este esquema de clasificación estricta podría traducirse en mediciones de resultados sustancialmente peores para los portadores de tumores residuales. Sin embargo, dado el hecho de que las complicaciones se produjeron con mayor frecuencia en el grupo de 5-ALA se precisarían estudios ajustados a riesgo (Stummer y col., 2011).
La monitorización intraoperatoria de las funciones neurológicas ha demostrado ser útil tanto en la preservación de la integridad funcional y el aumento de la “radicalidad '(De Witt y col., 2012).
La resección seguida de radioterapia se asocia con una supervivencia más larga que la radioterapia con biopsia sola (Devaux y col., 1993).
El tratamiento actual consiste en la resección quirúrgica máxima seguida de radioterapia y temozolomida ( Stupp y col., 2005, Stupp y col., 2009).
A pesar de este tratamiento agresivo, la mediana de supervivencia se mantiene aproximadamente en 14 meses.
El tratamiento quirúrgico va a depender de la localización del tumor la edad del paciente y el grado de Karnofski.
En localizaciones no elocuentes se realizará una citoreducción lo más amplia posible seguida de un régimen de radioterapia que consiste en una aplicación de 60 Gy (veinte Gy sobre el hecho tumoral y 40 Gy holocraneales).
Hoy en día la mayoría se operan usando sistemas de neuronavegación a partir de los datos 3D preoperatorios.
El tratamiento quimioterápico, particularmente con nitrosoureas, se ha mostrado sólo parcialmente eficiente.
Inmunoterapia (Jackson y col., 2011).
Otros tratamientos.-
Proton beam radiosurgery Boron-neutron capture Terapia génica etc………..
La sustancia P es el ligando principal de los receptores de neurocinina 1 (NK-1), que se expresan constantemente en los gliomas malignos.
El vector P 111In/90Y-DOTAGA se une a estos receptores y puede ser utilizado para el tratamiento local de tumores cerebrales (Kneifel 2007).
La radioterapia local con (213)Bi-DOTA-[Thi (8),Met(O (2)) (11)]-substance P es factible y puede representar un tratamiento innovador y eficaz para los gliomas de áreas elocuentes (Cordier 2010).
Biopsia estereotáxica en los siguientes casos: Tumores muy pequeños
Pacientes en mal estado para anestesia general.
En localizaciones elocuentes. (La diana debe ser el centro necrótico y el anillo hipercaptante).
Los corticosteroides siguen siendo el pilar para el manejo del edema cerebral causado desde la década de 1960 aunque el uso crónico puede causar un síndrome de Cushing iatrogénico (Wheeler y col., 2011).
Futuro
Receptor de EGFR conjugado con nanopartículas de óxido de hierro (Bouras y col., 2012).
Pronóstico
Se han identificado cinco factores pronósticos independientes de supervivencia:
Edad, Karnofsky Performance Scale (KPS), Grado de resección, Grado de necrosis, captación de contraste en la RM preoperatoria
Los pacientes con la metilación del promotor de la MGMT y resección completa tuvieron el mejor pronóstico.
El grado de resección actúa sinérgicamente con la radioquimioterapia concomitante y adyuvante, especialmente en pacientes con la metilación del promotor MGMT (Stummer y col., 2012).
Sin tratamiento, la mediana de supervivencia es de aproximadamente 3 meses (Walker y col., 1978).
Estos tumores están asociados con el tiempo de supervivencia más baja, que es de 1-2 años.
También se han implicado varios factores pronósticos que afectan el resultado a largo plazo en pacientes con glioblastoma multiforme.
Estos incluyen una edad más joven, sexo femenino, resección quirúrgica agresiva, componente oligodendroglial, glioblastoma de células gigantes, bajo índice de proliferación, p53 alta y bajo factor del receptor para positividad de EGFR.
La edad en el momento del diagnóstico inicial, la puntuación de Karnofsky, y el estado de metilación del promotor O (6)-metilguanina ADN-metiltransferasa son los predictores mejor documentados (Okita y col., 2012).
Stummer y col., añade la resección quirúrgica macroscópicamente completa (Stummer y col., 2012).
El objetivo de un enfoque neoadyuvante es la reducción de las células del tumor dentro de la masa tumoral y en la zona de infiltración (Cordier 2010), pero la resección quirúrgica completa más allá de los márgenes del tumor no se puede lograr en el glioblastoma multiforme (GBM), debido a la naturaleza infiltrante.
La combinación de la amplificación gen-EGFR y pérdida de heterozigosidad (LOH)del cromosoma 10, son de peor pronóstico.
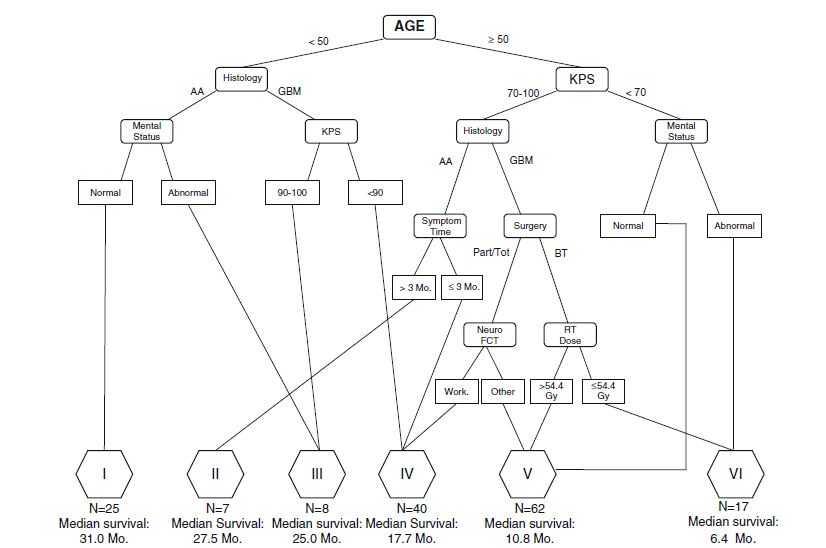
Escala de la RTOP-RPA (Radiation Therapy Oncology Group recursive partitioning analysis)
Los reingresos en los primeros 30 días tuvieron una supervivencia significativamente más corta 1).
Bibliografía
De Witt Hamer PC, Gil Robles S, Zwinderman aH, et al. Impact of intraoperative stimulation brain mapping on glioma surgery outcome: a meta-analysis. J Clin Oncol 2012;30(20):2559-2565.
Lacroix M, abi-Said D, Fourney DR, et al. a multivariate analysis of 416 patients with glioblastoma multiforme: prognosis, extent of resection, and survival. J Neurosurg 2001;95:190-198.
Pichlmeier U, Bink a, Schackert G, et al. Resection and survival in glioblastoma multiforme: an RTOG recursive partitioning analysis of aLa study patients. Neuro-oncol 2008;10:1025-1034.
Sanai N, Polley MY, McDermott MW et al. An extent of resection threshold for newly diagnosed glioblastomas. J Neurosurg 2011;115:3-8.
Stummer W, Tonn JC, Mehdorn HM, et al. Counterbalancing risks and gains from extended resections in malignant glioma surgery: a supplemental analysis from the randomized 5-aminolevulinic acid glioma resection study. Clinical article. J Neurosurg 2011;114:613-623. CrossRefMedline
Baldi, I, A Huchet, L Bauchet, and H Loiseau. 2010. “[Epidemiology of Glioblastoma].” Neuro-Chirurgie 56 (6) (December): 433–440. doi:10.1016/j.neuchi.2010.07.011.
Bouras, Alexandros, Milota Kaluzova, and Costas George Hadjipanayis. 2012. “192 Epidermal Growth Factor Receptor Antibody-conjugated Iron-oxide Nanoparticles: Therapeutic Targeting and Radiosensitivity Enhancement of Glioblastoma.” Neurosurgery 71 (2) (August): E574–575. doi:10.1227/01.neu.0000417782.45632.34.
Cordier, D, F Forrer, F Bruchertseifer, A Morgenstern, C Apostolidis, S Good, J Müller-Brand, H Mäcke, J C Reubi, y A Merlo. 2010. Targeted alpha-radionuclide therapy of functionally critically located gliomas with (213)Bi-DOTA-[Thi (8),Met(O (2)) (11)]-substance P: a pilot trial. European Journal of Nuclear Medicine and Molecular Imaging (Febrero 16). doi:10.1007/s00259-010-1385-5. http://www.ncbi.nlm.nih.gov/pubmed/20157707.
Cordier, Dominik, Flavio Forrer, Stefan Kneifel, Martin Sailer, Luigi Mariani, Helmut Mäcke, Jan Müller-Brand, y Adrian Merlo. 2010. Neoadjuvant targeting of glioblastoma multiforme with radiolabeled DOTAGA-substance P-results from a phase I study. Journal of Neuro-Oncology (Marzo 10). doi:10.1007/s11060-010-0153-5. http://www.ncbi.nlm.nih.gov/pubmed/20217458.
Devaux, B C, J R O’Fallon, and P J Kelly. 1993. “Resection, Biopsy, and Survival in Malignant Glial Neoplasms. A Retrospective Study of Clinical Parameters, Therapy, and Outcome.” Journal of Neurosurgery 78 (5) (May): 767–775. doi:10.3171/jns.1993.78.5.0767.
Franco-Hernández, C, V Martínez-Glez, and J A Rey. 2007. “[Biology molecular of glioblastomas].” Neurocirugía (Asturias, Spain) 18 (5) (October): 373-382.
Gousias, K, M Markou, S Voulgaris, A Goussia, P Voulgari, M Bai, K Polyzoidis, A Kyritsis, and Y Alamanos. 2009. “Descriptive epidemiology of cerebral gliomas in northwest Greece and study of potential predisposing factors, 2005-2007.” Neuroepidemiology 33 (2): 89-95. doi:10.1159/000222090.
Jackson, Christopher, Jacob Ruzevick, Jillian Phallen, Zineb Belcaid, and Michael Lim. 2011. “Challenges in immunotherapy presented by the glioblastoma multiforme microenvironment.” Clinical & Developmental Immunology 2011: 732413. doi:10.1155/2011/732413.
Jakola, Asgeir S, Sasha Gulati, Clemens Weber, Geirmund Unsgård, and Ole Solheim. 2011. “Postoperative deterioration in health related quality of life as predictor for survival in patients with glioblastoma: a prospective study.” PloS One 6 (12): e28592. doi:10.1371/journal.pone.0028592.
Jemal A, Siegel R, Xu J, et al. Cancer statistics, 2010. CA Cancer J Clin 2010;60:277e300
Khalatbari, Mahmoud Reza, Mehrdokht Hamidi, and Yashar Moharamzad. 2011. “Glioblastoma multiforme with very rapid growth and long-term survival in children: report of two cases and review of the literature.” Child’s Nervous System: ChNS: Official Journal of the International Society for Pediatric Neurosurgery 27 (8) (August): 1347-1352. doi:10.1007/s00381-011-1492-z.
Kneifel, Stefan, Peter Bernhardt, Helena Uusijärvi, Stephan Good, Ludwig Plasswilm, Carlos Buitrago-Téllez, Jan Müller-Brand, Helmut Mäcke, y Adrian Merlo. 2007. Individual voxelwise dosimetry of targeted 90Y-labelled substance P radiotherapy for malignant gliomas. European Journal of Nuclear Medicine and Molecular Imaging 34, no. 9 (Septiembre): 1388-1395. doi:10.1007/s00259-006-0351-8.
Márquez-Rivas, Javier, Gema Ramirez, Angela Ollero-Ortiz, Jorge Giménez-Pando, Juan Emmerich, Eduardo Quiroga-Cantero, Eloy Rivas, y Emilio Gómez-González. 2010. Initial Experience Involving Treatment and Retreatment With Carmustine Wafers in Combination With Oral Temozolomide: Long-term Survival in a Child With Relapsed Glioblastoma Multiforme. Journal of Pediatric Hematology/Oncology: Official Journal of the American Society of Pediatric Hematology/Oncology (Junio 2). doi:10.1097/MPH.0b013e3181e0d16b. http://www.ncbi.nlm.nih.gov/pubmed/20523247.
Motomura, Kazuya, Atsushi Natsume, Yugo Kishida, Hiroyuki Higashi, Yutaka Kondo, Yoko Nakasu, Tatsuya Abe, Hiroki Namba, Kenji Wakai, y Toshihiko Wakabayashi. 2011. «Benefits of interferon-β and temozolomide combination therapy for newly diagnosed primary glioblastoma with the unmethylated MGMT promoter: A multicenter study». Cancer 117 (8) (Abril 15): 1721-1730. doi:10.1002/cncr.25637.
Nguyen, Van, Jesse M Conyers, Dongqin Zhu, Denise M Gibo, Jay F Dorsey, Waldemar Debinski, and Akiva Mintz. 2011. “IL-13Rα2-Targeted Therapy Escapees: Biologic and Therapeutic Implications.” Translational Oncology 4 (6) (December): 390-400.
Okita, Yoshiko, Yoshitaka Narita, Yasuji Miyakita, Makoto Ohno, Shintaro Fukushima, Takamasa Kayama, and Soichiro Shibui. 2012. “Pathological Findings and Prognostic Factors in Recurrent Glioblastomas.” Brain Tumor Pathology (February 14). doi:10.1007/s10014-012-0084-2. http://www.ncbi.nlm.nih.gov/pubmed/22331317.
Phillips HS, Kharbanda S, Chen R, et al. Molecular subclasses of high-grade glioma predict prognosis, delineate a pattern of disease progression, and resemble stages in neurogenesis. Cancer Cell 2006;9:157e73.
Stratton MR, Campbell PJ, Futreal PA. The cancer genome. Nature 2009;458:719e24.
Stummer, Walter, Thomas Meinel, Christian Ewelt, Peter Martus, Olga Jakobs, Jörg Felsberg, and Guido Reifenberger. 2012. “Prospective Cohort Study of Radiotherapy with Concomitant and Adjuvant Temozolomide Chemotherapy for Glioblastoma Patients with No or Minimal Residual Enhancing Tumor Load After Surgery.” Journal of Neuro-Oncology (February 4). doi:10.1007/s11060-012-0798-3. http://www.ncbi.nlm.nih.gov/pubmed/22307805.
Stummer, Walter, Thomas Meinel, Christian Ewelt, Peter Martus, Olga Jakobs, Jörg Felsberg, and Guido Reifenberger. 2012. “Prospective Cohort Study of Radiotherapy with Concomitant and Adjuvant Temozolomide Chemotherapy for Glioblastoma Patients with No or Minimal Residual Enhancing Tumor Load After Surgery.” Journal of Neuro-oncology 108 (1) (May): 89–97. doi:10.1007/s11060-012-0798-3.
Stupp R, Mason WP, van den Bent MJ, et al. Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma. N Engl J Med 2005;352:987e96
Stupp R, Hegi ME, Mason WP, et al; European Organisation for Research and Treatment of Cancer Brain Tumour and Radiation Oncology Groups; National Cancer Institute of Canada Clinical Trials Group. Effects of radiotherapy with concomitant and adjuvant temozolomide versus radiotherapy alone on survival in glioblastoma in a randomised phase III study: 5-year analysis of the EORTC-NCIC trial. Lancet Oncol 2009;10:459e66.
Verhaak RG, Hoadley KA, Purdom E, et al. Integrated genomic analysis identifies clinically relevant subtypes of glioblastoma characterized by abnormalities in PDGFRA, IDH1, EGFR, and NF1. Cancer Cell 2010;17:98e110
Walker MD, Alexander E Jr, Hunt WE, et al. Evaluation of BCNU and/or radiotherapy in the treatment of anaplastic gliomas. A cooperative clinical trial. J Neurosurg 1978;49:333e43.
Wen PY, Kesari S. Malignant gliomas in adults. N Engl J Med 2008;359:492e507
Wheeler, Helen, Jason Black, Suzanne Webb, and Han Shen. 2011. “Dehiscence of Corticosteroid-Induced Abdominal Striae in a 14-Year-Old Boy Treated With Bevacizumab for Recurrent Glioblastoma.” Journal of Child Neurology (December 21). doi:10.1177/0883073811428007. http://www.ncbi.nlm.nih.gov/pubmed/22190499.
Zada, Gabriel, Aaron E Bond, Ya-Ping Wang, Steven L Giannotta, and Dennis Deapen. 2011. “Incidence Trends in the Anatomic Location of Primary Malignant Brain Tumors in the United States: 1992-2006.” World Neurosurgery (November 7). doi:10.1016/j.wneu.2011.05.05